¡Tu carrito está actualmente vacío!
¡Aliadas Inesperadas del Cáncer! Bacterias Dentro del Tumor Pueden Hacer que la Terapia Contra el Cáncer de Mama Falle
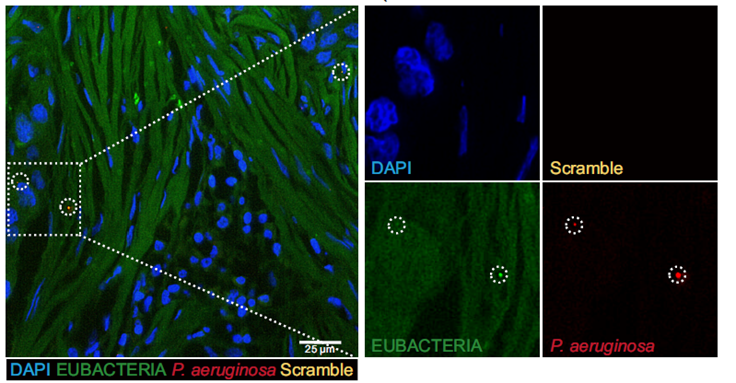
En Pocas Palabras:
El cáncer de mama HER2-positivo se trata comúnmente con trastuzumab, un anticuerpo que bloquea la proteína HER2 (ErbB2) en las células cancerosas. Sin embargo, muchos tumores desarrollan resistencia a este tratamiento. Un nuevo estudio ha descubierto una causa sorprendente: una bacteria común, Pseudomonas aeruginosa, que puede vivir dentro de los tumores de mama, libera una molécula de señalización (llamada 3oc) que “despierta” una vía de crecimiento alternativa en las células cancerosas (la vía del TGF-β). Esta vía activada, a su vez, reactiva la señalización de ErbB2 a pesar del trastuzumab, permitiendo que las células cancerosas sigan proliferando. Este hallazgo sugiere que las bacterias intratumorales pueden influir directamente en la eficacia de las terapias dirigidas, abriendo nuevas vías para combatir la resistencia a los tratamientos.
Molécula de 3oc
La Batalla Contra la Resistencia en el Cáncer de Mama
El cáncer de mama es una de las enfermedades más comunes y temidas a nivel mundial. Para un subtipo específico, conocido como HER2-positivo (o ErbB2-positivo), que afecta aproximadamente al 20% de las pacientes y se caracteriza por una alta agresividad, el desarrollo del anticuerpo monoclonal trastuzumab (Herceptin) supuso una revolución terapéutica. El trastuzumab actúa bloqueando la proteína ErbB2, que está sobreexpresada en la superficie de estas células cancerosas y promueve su crecimiento descontrolado. A pesar de su éxito inicial, un problema persistente es que muchas pacientes desarrollan resistencia al trastuzumab, lo que limita severamente su eficacia a largo plazo. Las causas de esta resistencia son complejas y no del todo comprendidas. Un nuevo y sorprendente estudio publicado en PNAS por Gege Qin, Xiaohong Fang, Wei Zhou y colaboradores de China, ha identificado un actor inesperado en este drama: las bacterias que residen dentro del propio tumor pueden jugar un papel directo en promover la resistencia al trastuzumab.
El Microbioma del Tumor: Un Nuevo Jugador en el Campo de Batalla
Durante mucho tiempo, se consideró que la mayoría de los tumores, fuera del tracto gastrointestinal o respiratorio, eran estériles. Sin embargo, investigaciones recientes han revelado la existencia de un microbioma intratumoral, una comunidad de bacterias que pueden vivir dentro de los tejidos cancerosos. Si bien su función exacta está comenzando a explorarse, este estudio proporciona una de las primeras evidencias claras de cómo estas bacterias pueden influir directamente en la respuesta a una terapia dirigida.
Los investigadores se centraron en Pseudomonas aeruginosa, una bacteria oportunista que se ha encontrado con relativa abundancia en tumores de mama. Esta bacteria es conocida por utilizar un sistema de comunicación llamado “quorum sensing”, donde libera moléculas de señalización para coordinar su comportamiento. Una de estas moléculas es la N-(3-oxo-dodecanoil)-L-homoserina lactona (3oc).
El Descubrimiento: Cómo una Molécula Bacteriana Sabotea la Terapia
El equipo demostró que la molécula 3oc, liberada por P. aeruginosa, tiene un efecto directo y perjudicial sobre las células de cáncer de mama HER2-positivo tratadas con trastuzumab:
- Induce Resistencia: La presencia de 3oc hizo que las células cancerosas se volvieran significativamente menos sensibles al trastuzumab. Necesitaban dosis mucho más altas del fármaco para frenar su proliferación.

- No es Toxicidad Directa: A diferencia de su efecto sobre algunas células inmunes (donde 3oc puede inducir apoptosis o muerte celular), esta molécula no mataba directamente a las células cancerosas ni afectaba su viabilidad por sí sola en las concentraciones estudiadas. Su efecto era específico en el contexto del tratamiento con trastuzumab.

- Mecanismo Molecular Revelado: El estudio desveló el elegante mecanismo detrás de esta resistencia:
- Activación de la Vía del TGF-β: La molécula 3oc, al parecer interactuando con la membrana celular y alterando la estructura de las balsas lipídicas, provoca la dimerización espontánea del receptor tipo II del factor de crecimiento transformante beta (TβRII). Esto ocurre ¡incluso en ausencia del ligando natural TGF-β1!
- Reactivación de ErbB2: Esta activación “forzada” de la vía del TGF-β, a su vez, desencadena una cascada de señales que lleva a la fosforilación (activación) de ErbB2 y sus vías de señalización descendentes (como MAPK y PI3K/Akt), que son cruciales para la proliferación y supervivencia celular.
- Eludiendo el Bloqueo: Esencialmente, la molécula bacteriana 3oc proporciona una “ruta de escape” que permite a las células cancerosas reactivar la señalización de ErbB2 a pesar de que el trastuzumab está intentando bloquearla.

Confirmación Clínica: Bacterias y Resistencia en Pacientes
Para validar la relevancia clínica de estos hallazgos, los investigadores analizaron muestras de tumores de mama de pacientes:
- Detectaron la presencia de P. aeruginosa en un porcentaje de los tumores.
- Encontraron una correlación clínica entre la colonización por P. aeruginosa y una peor respuesta al tratamiento con trastuzumab (pacientes con mayor abundancia de la bacteria tenían menos probabilidad de alcanzar una remisión patológica completa).
- Además, utilizando técnicas sensibles de espectrometría de masas, detectaron la molécula 3oc directamente en los tejidos tumorales congelados, y estimaron que su concentración local podría alcanzar niveles suficientes para inducir los efectos observados in vitro.

Implicaciones y Futuro: Un Nuevo Enfoque para Combatir la Resistencia
Este estudio es sumamente importante porque:
- Nuevo Mecanismo de Resistencia: Identifica un mecanismo extrínseco, mediado por bacterias intratumorales, que contribuye a la resistencia a una terapia dirigida clave en cáncer de mama.
- Interacción Directa Bacteria-Tumor: Proporciona evidencia sólida de una comunicación química directa entre bacterias residentes en el tumor y las células cancerosas, con consecuencias funcionales para la respuesta al tratamiento.
- Implicaciones Terapéuticas:
- Sugiere que la modulación del microbioma intratumoral podría ser una nueva estrategia para mejorar la eficacia del trastuzumab y otras terapias contra el cáncer.
- Plantea la posibilidad de que el uso de antibióticos específicos para eliminar o reducir la carga de P. aeruginosa en ciertos tumores podría ayudar a prevenir o revertir la resistencia.
- Abre la puerta a la búsqueda de inhibidores de la señalización por 3oc o de la vía del TGF-β como coadyuvantes en la terapia del cáncer de mama HER2-positivo.
- Más Allá del Cáncer de Mama: Dado que 3oc también mostró efectos en líneas celulares de cáncer gástrico, este fenómeno podría ser relevante para otros tipos de cáncer donde ErbB2 es una diana terapéutica y donde P. aeruginosa u otras bacterias productoras de moléculas similares puedan estar presentes.

Conclusión: Escuchando las Conversaciones Secretas Dentro del Tumor
El trabajo de Qin, Fang, Zhou y colaboradores nos sumerge en el fascinante y cada vez más relevante mundo del microbioma tumoral. Al demostrar cómo una simple molécula de señalización bacteriana puede sabotear una terapia anticancerígena dirigida, este estudio subraya la importancia de considerar el tumor no como una masa aislada de células malignas, sino como un ecosistema complejo donde las interacciones entre las células cancerosas y los microorganismos residentes pueden tener un impacto profundo en el curso de la enfermedad y la eficacia del tratamiento. Estos hallazgos nos instan a “escuchar” estas conversaciones secretas para desarrollar estrategias terapéuticas más inteligentes y efectivas.
Referencia del Artículo:
Qin, G., Shao, X., Liu, X., Xu, J., Wang, X., Wang, W., … & Fang, X. (2025). A signaling molecule from intratumor bacteria promotes trastuzumab resistance in breast cancer cells. PNAS, 122(2), e2421710122. https://doi.org/10.1073/pnas.2421710122
(Nota: Los nombres de los autores han sido acortados por brevedad en la nota, pero la referencia completa está disponible en el artículo original).
AI bacterias Biología Sintética CRISPR cáncer envejecimiento Escherichia coli evolución Microbioma microbiota regulación resistencia salud VIH virus
Ultimos Productos
-
Curso de Organismos Modelo en Biología Molecular Febrero 2025
El precio original era: $75.00.$57.00El precio actual es: $57.00. -
Masterclass: Dinámica y Composición de los Condensados Biomoleculares
El precio original era: $80.00.$60.00El precio actual es: $60.00.
Buscar
Últimos Posts
Últimos Comentarios
Categorías
Archivos
- marzo 2026 (5)
- febrero 2026 (15)
- enero 2026 (21)
- diciembre 2025 (20)
- noviembre 2025 (16)
- octubre 2025 (21)
- septiembre 2025 (17)
- agosto 2025 (17)
- julio 2025 (19)
- junio 2025 (24)
- mayo 2025 (26)
- abril 2025 (49)
- marzo 2025 (20)
- febrero 2025 (10)
- enero 2025 (7)
- diciembre 2024 (8)
- noviembre 2024 (23)
- octubre 2024 (7)
Palabras clave
Sígue las noticias
Te invitamos a registrar tus datos como tu correo electrónico para que puedas recibir las últimas noticias y anuncios de Biología Molecular México

By signing up, you agree to the our terms and our Privacy Policy agreement.