¡Tu carrito está actualmente vacío!
Edición precisa de receptores de células T reguladoras para la enfermedad celíaca
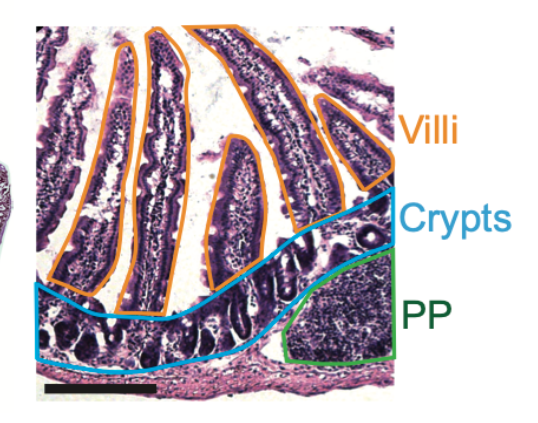
¿Qué es la enfermedad celíaca? La enfermedad celíaca es un trastorno inflamatorio crónico del intestino delgado que afecta aproximadamente al 1% de la población mundial. Se desencadena por una respuesta inmunológica anormal a las proteínas del gluten presentes en trigo, cebada y centeno. Esta respuesta provoca daño intestinal y producción de autoanticuerpos, llevando a síntomas digestivos y complicaciones sistémicas. Hasta ahora, el único tratamiento disponible es seguir una dieta libre de gluten de por vida, lo cual es complicado, costoso y no siempre completamente eficaz.
¿Qué propone este estudio? Investigadores han explorado un enfoque innovador: el uso de células T reguladoras (Tregs) diseñadas específicamente para reconocer y suprimir la respuesta autoinmune contra el gluten. Las Tregs son células inmunitarias clave que previenen respuestas exageradas del sistema inmunológico y mantienen la tolerancia. Al modificar sus receptores (TCR) para que reconozcan epítopos específicos del gluten presentados por la molécula HLA-DQ2.5 (presente en más del 90% de los pacientes celíacos), se busca frenar la respuesta inflamatoria de manera específica.

dominantes del gluten (DQ2.5-glia-α1a y DQ2.5-glia-α2). Estos TCRs fueron introducidos en células T humanas y murinas mediante edición genética precisa, reemplazando el receptor endógeno por el receptor diseñado. Las células T efectores (Teffs) y las Tregs modificadas fueron evaluadas tanto in vitro como en modelos de ratón transgénicos que expresan HLA-DQ2.5.
Resultados clave:
- Migración específica: Las células T efectores diseñadas (eTeffs) migraron específicamente hacia el intestino y los ganglios linfáticos relacionados tras exposición al gluten, demostrando que reconocen eficazmente los epítopos objetivo.
- Supresión antigénica: Las eTregs diseñadas mostraron una capacidad de supresión altamente eficaz sobre las eTeffs, no solo frente al epítopo para el cual fueron diseñadas, sino también sobre células que reconocen otros epítopos, evidenciando un efecto de supresión por vecindad.
- Dependencia del antígeno: Las Tregs poli-clonales no lograron suprimir la respuesta, destacando que la activación específica por antígeno es esencial para la eficacia terapéutica.
- Posible efecto terapéutico: En los modelos murinos, las eTregs no solo redujeron la proliferación de células T inflamatorias, sino que también impidieron su migración hacia el intestino, lo cual es clave para prevenir el daño intestinal.

¿Por qué es importante este avance? Esta investigación representa un paso significativo hacia una terapia celular personalizada y específica para la enfermedad celíaca. La posibilidad de inducir tolerancia inmunológica sin necesidad de inmunosupresión general ni dietas extremadamente restrictivas abre un camino innovador que podría ser aplicado en otras enfermedades autoinmunes.
Conclusión El estudio demuestra que las Tregs diseñadas para reconocer epítopos clave del gluten pueden frenar la respuesta autoinmune en celiacos. Aunque los resultados son preliminares y obtenidos en modelos animales, representan una base sólida para futuros ensayos clínicos que podrían transformar el tratamiento de la enfermedad celíaca.
Referencia: Porret R, Alcaraz-Serna A, Peter B, Bernier-Latmani J, Cecchin R, Alfageme-Abello O, Ermellino L, Hafezi M, Pace E, du Pré MF, Lana E, Golshayan D, Velin D, Eyquem J, Tang Q, Petrova TV, Coukos G, Irving M, Pot C, Pantaleo G, Sollid LM, Muller YD. T cell receptor precision editing of regulatory T cells for celiac disease. Sci Transl Med. 2025 Mar 19;17(790):eadr8941. doi: 10.1126/scitranslmed.adr8941.
AI bacterias Biología Sintética CRISPR cáncer envejecimiento Escherichia coli evolución Microbioma microbiota regulación resistencia salud VIH virus
Ultimos Productos
-
Curso de Organismos Modelo en Biología Molecular Febrero 2025
El precio original era: $75.00.$57.00El precio actual es: $57.00. -
Masterclass: Dinámica y Composición de los Condensados Biomoleculares
El precio original era: $80.00.$60.00El precio actual es: $60.00.
Buscar
Últimos Posts
Últimos Comentarios
Categorías
Archivos
- marzo 2026 (5)
- febrero 2026 (15)
- enero 2026 (21)
- diciembre 2025 (20)
- noviembre 2025 (16)
- octubre 2025 (21)
- septiembre 2025 (17)
- agosto 2025 (17)
- julio 2025 (19)
- junio 2025 (24)
- mayo 2025 (26)
- abril 2025 (49)
- marzo 2025 (20)
- febrero 2025 (10)
- enero 2025 (7)
- diciembre 2024 (8)
- noviembre 2024 (23)
- octubre 2024 (7)
Palabras clave
Sígue las noticias
Te invitamos a registrar tus datos como tu correo electrónico para que puedas recibir las últimas noticias y anuncios de Biología Molecular México

By signing up, you agree to the our terms and our Privacy Policy agreement.