¡Tu carrito está actualmente vacío!
El Talón de Aquiles Oculto de la Leucemia: Cómo sus Propios Errores Genéticos la Hacen Vulnerable
Las leucemias mieloides agudas (LMA) y los síndromes mielodisplásicos (SMD) son cánceres de la sangre agresivos y a menudo difíciles de tratar. Aunque ha habido avances, muchos pacientes recaen o no responden a las terapias disponibles. La inmunoterapia, que utiliza el propio sistema inmunitario del paciente para atacar el cáncer, es una estrategia prometedora, pero encontrar blancos específicos únicamente en las células leucémicas (y no en las sanas) ha sido un gran desafío.
Ahora, un equipo de investigadores de centros punteros como el Memorial Sloan Kettering Cancer Center y el Fred Hutchinson Cancer Center ha descubierto una nueva clase de blancos terapéuticos derivados de un error fundamental que cometen estas células cancerosas. Su trabajo, publicado en la prestigiosa revista Cell, revela cómo mutaciones comunes en la maquinaria de “corte y empalme” del ARN (splicing) generan “neoantígenos” únicos que pueden ser reconocidos por el sistema inmunitario.
Errores de “Corte y Empalme” (Splicing) en la Leucemia
Nuestros genes contienen instrucciones (ADN) que se copian en mensajes (ARN). Antes de que estos mensajes se traduzcan en proteínas, necesitan ser editados: se eliminan fragmentos no codificantes (intrones) y se unen los fragmentos codificantes (exones). Este proceso se llama splicing y es realizado por una maquinaria celular compleja conocida como spliceosoma.
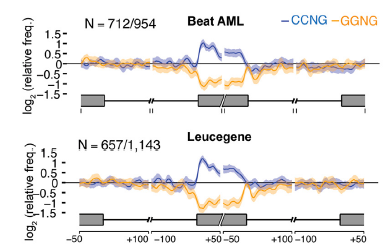
Resulta que en una gran proporción de pacientes con LMA y SMD (hasta un 70%), esta maquinaria de splicing tiene mutaciones en algunos de sus componentes clave (genes como SRSF2 o ZRSR2). Estas mutaciones no impiden que el splicing ocurra, pero hacen que la maquinaria cometa errores predecibles y recurrentes. Produce versiones de ARN “mal empalmadas” (mis-splicing) que son diferentes a las que se encuentran en células normales.

Del Error a la Bandera: Nacen los Neoantígenos
Aquí viene la clave: cuando la célula traduce estas moléculas de ARN mal empalmadas, produce proteínas o fragmentos de proteína anormales que son completamente nuevos y únicos de las células leucémicas. Si pequeños fragmentos (péptidos) de estas proteínas anormales se presentan en la superficie celular (a través de moléculas HLA), actúan como neoantígenos: banderas moleculares que gritan “¡Soy una célula cancerosa!” al sistema inmunitario.


Lo emocionante es que, como las mutaciones en SRSF2 y ZRSR2 son comunes y causan errores de splicing similares en muchos pacientes, los neoantígenos resultantes también son “públicos”, es decir, compartidos entre diferentes individuos con la misma mutación.
Encontrando las Armas: Linfocitos T y sus Receptores (TCRs)
Los investigadores identificaron una serie de estos neoantígenos recurrentes derivados del mis-splicing. Luego se preguntaron: ¿puede el sistema inmunitario reconocerlos?
- Descubrieron que los pacientes con leucemia sí tenían linfocitos T (las células inmunitarias asesinas) en su sangre capaces de reconocer estos neoantígenos, pero a menudo estas células estaban disfuncionales o “agotadas”.
- Utilizando técnicas sofisticadas, lograron aislar los “detectores” moleculares de estos linfocitos T (los receptores de células T o TCRs) que reconocían específicamente a los neoantígenos. Encontraron TCRs particularmente potentes, a menudo provenientes de donantes sanos o de pacientes que habían superado la leucemia tras un trasplante de médula ósea.
La Prueba de Fuego: Terapia Celular Dirigida
El paso final fue probar si estos TCRs podían usarse como arma terapéutica. Tomaron linfocitos T normales y los modificaron genéticamente para que expresaran los TCRs específicos contra los neoantígenos. ¡Los resultados fueron contundentes!
- Estas células T modificadas con TCRs eran capaces de reconocer y destruir específicamente las células de leucemia que portaban la mutación SRSF2 (y por tanto, presentaban el neoantígeno) en cultivos de laboratorio.
- En modelos animales (ratones), la infusión de estas células T modificadas logró controlar eficazmente el crecimiento del tumor leucémico.
Conclusión: Una Nueva Ventana Terapéutica
Este estudio es un gran avance porque identifica una fuente completamente nueva de blancos terapéuticos “públicos” para leucemias mieloides, basados en las consecuencias moleculares de mutaciones muy comunes en los factores de splicing. Proporciona una fuerte prueba de concepto para el desarrollo de terapias celulares con TCRs modificados dirigidas a estos neoantígenos derivados del mis-splicing. Es una estrategia elegante que, en esencia, utiliza los propios errores genéticos del cáncer para diseñar un ataque inmunitario altamente específico y potente contra él. ¡Una nueva esperanza en la lucha contra estas difíciles enfermedades!
Referencia: Kim, W.J., Crosse, E.I., De Neef, E., et al. (2025). Mis-splicing-derived neoantigens and cognate TCRs in splicing factor mutant leukemias. Cell, 188, 1–19. DOI: 10.1016/j.cell.2025.03.047 (Nota: El DOI y fecha exacta de publicación final pueden variar)
AI bacterias Biología Sintética CRISPR cáncer envejecimiento Escherichia coli evolución Microbioma microbiota regulación resistencia salud VIH virus
Ultimos Productos
-
Curso de Organismos Modelo en Biología Molecular Febrero 2025
El precio original era: $75.00.$57.00El precio actual es: $57.00. -
Masterclass: Dinámica y Composición de los Condensados Biomoleculares
El precio original era: $80.00.$60.00El precio actual es: $60.00.
Buscar
Últimos Posts
Últimos Comentarios
Categorías
Archivos
- marzo 2026 (5)
- febrero 2026 (15)
- enero 2026 (21)
- diciembre 2025 (20)
- noviembre 2025 (16)
- octubre 2025 (21)
- septiembre 2025 (17)
- agosto 2025 (17)
- julio 2025 (19)
- junio 2025 (24)
- mayo 2025 (26)
- abril 2025 (49)
- marzo 2025 (20)
- febrero 2025 (10)
- enero 2025 (7)
- diciembre 2024 (8)
- noviembre 2024 (23)
- octubre 2024 (7)
Palabras clave
Sígue las noticias
Te invitamos a registrar tus datos como tu correo electrónico para que puedas recibir las últimas noticias y anuncios de Biología Molecular México

By signing up, you agree to the our terms and our Privacy Policy agreement.