📝 RESUMEN
La enfermedad de Huntington es devastadora en parte porque la proteína tóxica mutante (mHTT) tiene la capacidad de “contagiar” a células sanas vecinas. Una nueva investigación publicada en Science Advances revela exactamente cómo ocurre este secuestro celular: mediante la formación de “nanotubos de túnel” (TNTs) coordinados por un complejo de proteínas Rhes y Slc4a7. Al descubrir este mecanismo, los científicos lograron bloquear farmacológica y genéticamente la formación de estos túneles, reduciendo drásticamente la propagación de la proteína tóxica en cerebros de ratones vivos. Este hallazgo convierte a Slc4a7 en un blanco terapéutico sin precedentes para detener el progreso de la enfermedad.

1. Autopistas Tóxicas: El Problema de la Propagación 🌉🦠
¡GRACIAS POR LEER NUESTRAS NOTICIAS! ¿Nos invitas un cáfe? ☕
- En el cerebro de los pacientes con Huntington, la proteína mutante mHTT no se queda aislada, sino que viaja de una neurona a otra.

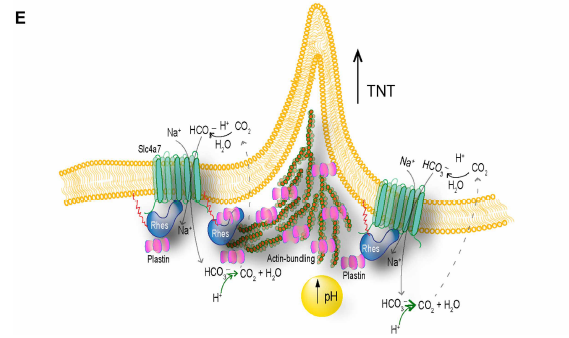
- Las células construyen “nanotubos de túnel” (TNTs), que son estructuras membranosas larguísimas y delgadas basadas en actina que funcionan como puentes directos entre los citoplasmas.

- Investigaciones previas ya habían señalado a la proteína Rhes (enriquecida en el cuerpo estriado del cerebro) como la reguladora clave que orquesta la creación de estos túneles y la transmisión de la mHTT.

2. El Cómplice Descubierto: La Proteína Slc4a7 🕵️♂️🔍
- Para entender cómo Rhes construye estas autopistas, los investigadores utilizaron espectrometría de masas (LC-MS/MS) para analizar qué otras proteínas de la membrana le ayudaban.
- Descubrieron que su principal socio es Slc4a7, un cotransportador de bicarbonato de sodio cuya función normal es regular el pH (la acidez) dentro de la célula.

3. Saboteando la Construcción de los Puentes 🚧⚡
- Rhes se une directamente a Slc4a7 y modula el pH intracelular local, lo cual es un paso crítico para facilitar la formación de los nanotubos.
- Para que Rhes pueda anclarse a la membrana y unirse a Slc4a7, requiere de una modificación lipídica llamada farnesilación.
- Los investigadores demostraron que, al usar moléculas para inhibir a Slc4a7 (como el compuesto DIDS) o al bloquear la farnesilación de Rhes, la formación de los túneles se colapsa y la transferencia de la proteína mHTT entre células se suprime de manera contundente.

4. De la Placa de Petri al Cerebro Vivo 🐁🧠
- Para confirmar que esto funciona en un organismo completo, el equipo utilizó ratones genéticamente modificados para no tener la proteína Slc4a7 (Slc4a7 knockout).
- Al inyectar la proteína mutante del Huntington en el cuerpo estriado de estos ratones, observaron que la transmisión de célula a célula se redujo notablemente en comparación con los ratones normales.

- Este descubrimiento destapa un eje de señalización (Rhes-Slc4a7) totalmente desconocido hasta ahora, posicionando a Slc4a7 como una diana farmacológica ideal para limitar la propagación del daño en pacientes con Huntington.

📚 REFERENCIA BIBLIOGRÁFICA
Dagar, S., Fernandez, A., Ramírez-Jarquín, U. N., Lopez-Huerta, V. G., Mirza, E., Mohapatra, C., Zuniga, I., Urban, N. T., Crynen, G., Tsaprailis, G., & Subramaniam, S. (2026). Membrane-associated Rhes-Slc4a7 complex orchestrates tunneling nanotube formation and mutant Huntingtin spread. Science Advances, 12, eaea1226. https://doi.org/10.1126/sciadv.aea1226