📝 RESUMEN
Para que las proteínas realicen sus funciones vitales, necesitan cambiar de forma. Aunque tecnologías como la criomicroscopía electrónica (cryo-EM) nos permiten obtener asombrosas “fotografías” tridimensionales de estos estados, simular la “película” que los conecta ha sido casi imposible para complejos gigantes debido a los inmensos costos computacionales. Ahora, científicos han desarrollado eBDIMS2, un algoritmo revolucionario con escalado casi lineal que permite simular transiciones de megaproteínas (como la ATP sintasa o la proteína Spike del coronavirus) en una computadora de escritorio estándar, coincidiendo con la precisión de simulaciones masivas y abriendo una nueva era para el diseño de fármacos.
🧪 Problemas de dinámica, ¿cómo tener la historia completa?
¡GRACIAS POR LEER NUESTRAS NOTICIAS! ¿Nos invitas un cáfe? ☕
1. El Problema: Tenemos las Fotos, pero nos Falta la Película 📸🎬
Las proteínas son máquinas dinámicas; se abren, se cierran y giran en respuesta a señales celulares. Hoy en día, técnicas avanzadas nos proporcionan estructuras detalladas de estos estados inactivos o activos. El problema es que los métodos computacionales clásicos, como la Dinámica Molecular (MD), escalan de forma cuadrática ($N^2$) según el tamaño del sistema. Esto significa que visualizar cómo una proteína gigante (>300 kDa) pasa del punto A al punto B exige recursos de supercomputación que muy pocos laboratorios en el mundo pueden pagar.
2. La Solución: eBDIMS2 al Rescate 💻⚡
Para superar esta barrera, los investigadores crearon eBDIMS2. Este algoritmo integra Modelos de Redes Elásticas (ENM) de grano grueso con simulaciones de Dinámica Browniana.

- El gran truco: Mediante un esquema optimizado de cortes y paralelización, el algoritmo logró una dependencia casi lineal con respecto al tamaño del sistema.
- Lo que antes tomaba días o meses en clústeres masivos, ahora se puede realizar en cuestión de horas en una simple computadora de escritorio, sin límite real en el tamaño o la arquitectura de la proteína.
3. Pruebas de Estrés: Modelando a los Gigantes Celulares 🏋️♂️🦠
Para probar su poder, los científicos enfrentaron a eBDIMS2 a los “pesos pesados” de la biología:
- La Chaperonina GroEL (~400 kDa): eBDIMS2 logró simular su apertura en apenas 1 hora con una asombrosa precisión, mientras que otros algoritmos colapsaban, deformaban la estructura o tardaban más de 12 horas.
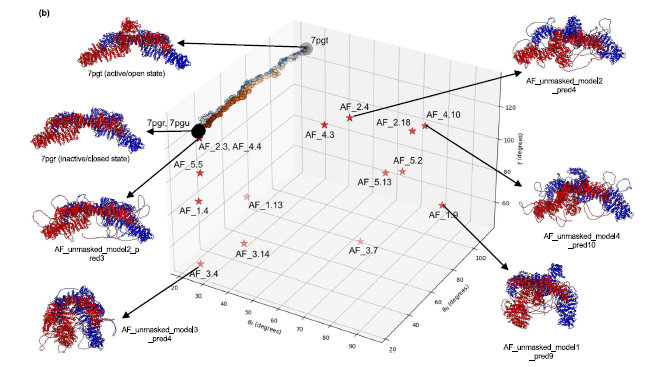
- Motores y Virus: El método capturó sin problemas transiciones complejísimas, como el intrincado movimiento rotatorio de las ATP sintasas o la apertura de la proteína Spike del SARS-CoV-2. * Sus resultados no fueron meras suposiciones geométricas: eBDIMS2 predice caminos que visitan de forma espontánea los estados intermedios reales detectados en experimentos y coincide con las costosísimas simulaciones atómicas (como Targeted MD).

4. Un Impacto Real en la Medicina del Futuro 🌍💊
La gran utilidad de eBDIMS2 radica en su aplicación práctica.
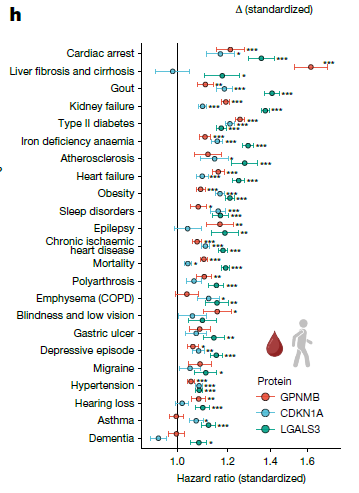
Muchas megaproteínas analizadas en este estudio están involucradas en enfermedades críticas como el cáncer, la tuberculosis y diversos trastornos musculares. Al poder generar rápidamente estas “películas” de transición, los investigadores pueden descubrir bolsillos o sitios ocultos transitorios (estados intermedios) que servirán como blancos perfectos para el desarrollo de nuevos medicamentos.

📚 REFERENCIA BIBLIOGRÁFICA
Scaramozzino, D., Lee, B. H., & Orellana, L. (2026). Efficient sampling of large-scale transition pathways and intermediate conformations in sub-mesoscopic protein complexes. Nature Communications, 17, 2202. https://doi.org/10.1038/s41467-026-69809-y