Resumen
El presente reporte analiza el estudio de Põder et al. (2026), el cual demuestra que el control efectivo de la Diabetes Tipo 1 (DT1) en modelos animales no solo depende del incremento de las células T reguladoras (Tregs), sino de la estabilidad y persistencia de dicho aumento. Mientras que los tratamientos actuales con dosis bajas de IL-2 suelen generar picos oscilantes de Tregs, el uso de la proteína de fusión mIL-2/CD25, administrada dos veces por semana, logró una elevación sostenida que restableció el sistema inmune, protegió las células β pancreáticas y redujo la expansión de células T autorreactivas.

1. El Desafío de la Inestabilidad Inmune 📉
¡GRACIAS POR LEER NUESTRAS NOTICIAS! ¿Nos invitas un cáfe? ☕
Históricamente, el uso de IL-2 recombinante (rIL-2) para tratar enfermedades autoinmunes ha enfrentado obstáculos debido a su vida media corta.

- Las dosis diarias de rIL-2 provocan una señalización intermitente, lo que genera niveles de Tregs que oscilan (suben y bajan rápidamente).
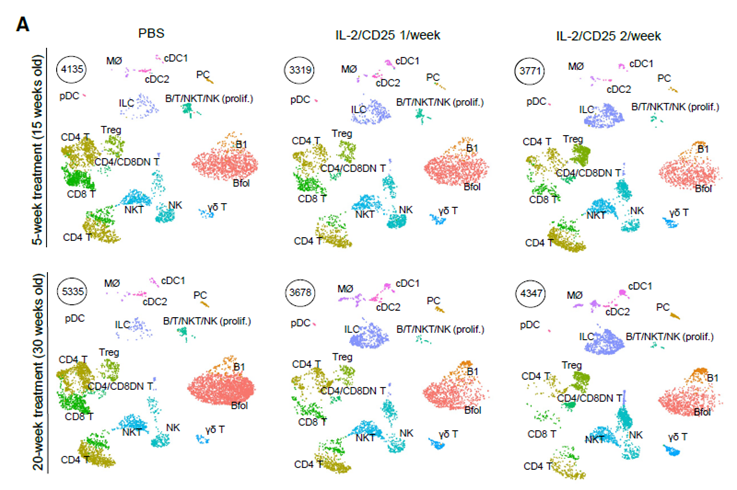
- El estudio comparó un régimen de mIL-2/CD25 una vez por semana (oscilante) frente a dos veces por semana (continuo).
- Resultado: Solo el aumento continuo logró mantener a casi todos los ratones normoglucémicos de forma duradera.

2. Remodelación del Paisaje Isletico 🧬
La administración sostenida de mIL-2/CD25 no solo afectó a las Tregs, sino que transformó todo el microambiente de los islotes pancreáticos:
- Reducción de Efectoras: Se observó una disminución drástica de múltiples subtipos de células T efectoras CD4+ y CD8+, responsables del ataque autoinmune.
- Nuevos Actores Regulatorios: El ambiente de los islotes pasó a estar dominado por Tregs, células linfoides innatas tipo 2 (ILC2) y células Natural Killer regulatorias (regNK).
- Reparación Tisular: Las Tregs y células Th2 en este modelo expresaron factores como Anfiregulina (AREG), TGF-β y Furina, asociados con la reparación de tejidos y la preservación de la función de las células β.

3. Impacto en el Repertorio de Receptores T (TCR) 🔍
Mediante secuenciación de ARN de célula única (scRNA-seq) y TCR, se descubrió que:
- El tratamiento reduce rápidamente la expansión clonal de las células T que reconocen antígenos propios (como la insulina).
- No hubo evidencia de que las células efectoras se “convirtieran” en Tregs; más bien, el tratamiento favoreció la expansión de Tregs ya existentes con capacidades supresoras optimizadas.
- Al suspender el tratamiento, el infiltrado inmune regresó gradualmente a un estado inflamatorio, lo que subraya la necesidad de una estimulación prolongada.
4. Implicaciones Clínicas 🏥
Este descubrimiento sugiere un cambio de paradigma en las terapias de inmunotolerancia:
- Más allá de la rIL-2: Las proteínas de fusión o muteínas de IL-2 con vida media prolongada son superiores para mantener la ventana terapéutica.
- Dosificación Crítica: Para enfermedades como la DT1 o el Lupus, se debe evitar el diseño de ensayos clínicos con periodos de descanso prolongados que permitan la caída de los niveles de Tregs.
Bibliografía
- Põder, J., Yu, A., Ding, Y., et al. (2026). Durable control of autoimmunity requires sustained stimulation of regulatory T cells. Cell Reports, 45, 117292. https://doi.org/10.1016/j.celrep.2026.117292.












Deja una respuesta