📝 RESUMEN
La bacteria Escherichia coli es el “caballo de batalla” de la biotecnología, pero su metabolismo natural desperdicia carbono en forma de CO2 durante la fermentación. Para solucionar esto, un equipo de investigadores ha logrado insertar la maquinaria central de la fotosíntesis (el ciclo de Calvin, incluida la famosa enzima Rubisco) en E. coli. El gran reto era evitar que la eficiente glucólisis natural “aplastara” a este nuevo sistema. Mediante una represión genética precisa (CRISPRi) y la eliminación de rutas energéticas, lograron una coexistencia armónica: la bacteria ahora consume glucosa con vigor mientras recicla su propio CO2, lo que abre la puerta a bioprocesos industriales mucho más eficientes y ecológicos.
1. El Reto: El Desperdicio en la Fábrica Celular 🏭💨
¡GRACIAS POR LEER NUESTRAS NOTICIAS! ¿Nos invitas un cáfe? ☕
En la naturaleza, los organismos suelen ser heterótrofos (comen compuestos orgánicos, como nosotros o E. coli) o autótrofos (fijan el CO2 del aire, como las plantas). En la biotecnología, usamos bacterias alimentadas con glucosa para producir todo tipo de productos, desde medicinas hasta plásticos. El problema es que la glucólisis (la ruta que rompe la glucosa) es tan eficiente evolutivamente que, durante el proceso, gran parte del carbono se escapa a la atmósfera como CO2 ¿La solución ideal? Un metabolismo “mixótrofo”: la bacteria come glucosa, pero reabsorbe el CO2 que produce.

2. Insertando el “Motor de las Plantas” en una bacteria 🌱⚙️
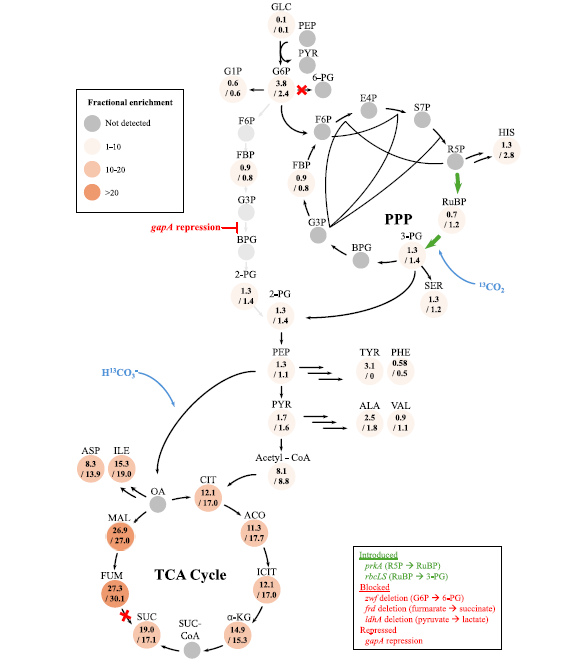
Para lograrlo, los científicos introdujeron en E. coli las dos enzimas clave del ciclo de Calvin-Benson-Bassham (CBB): la PrkA y la Rubisco. Esto creó una vía sintética capaz de fijar CO2. Sin embargo, encender este motor no es suficiente; la glucólisis natural es tan dominante que acapara todos los recursos de la célula. Había que “frenar” la glucólisis para que el nuevo ciclo de Calvin pudiera competir.
3. Hackeando el Sistema con CRISPRi y “Válvulas” de Energía ✂️🔋
Los investigadores usaron una estrategia en dos frentes:
- Freno selectivo: Usaron CRISPR de interferencia (CRISPRi) para reprimir el gen gapA, creando un “cuello de botella” en la glucólisis.
- Corte de suministros: Eliminaron rutas fermentativas que consumen poder reductor (los genes ldhA y frd, que producen lactato y succinato).
Al bloquear estas rutas normales, obligaron a la célula a depender de la nueva vía basada en Rubisco. ¡Y funcionó! El ciclo de Calvin no solo fijó CO2, sino que actuó como amortiguador metabólico: al producir moléculas clave justo después del cuello de botella de la glucólisis, logró restaurar el equilibrio.

4. Una “Armonía” Metabólica para el Futuro 🌍♻️
El resultado es una E. coli reprogramada que exhibe una “armonía” entre ambas rutas. La cepa modificada logró consumir glucosa de forma robusta (170 mg L^-1 h^-1), lo que derivó en el 10% de esa glucosa a través de la vía de Rubisco y en una tasa de fijación de CO2 de 5.0 mg L^-1 h^-1. Este metabolismo reconfigurado produce grandes cantidades de piruvato y acetato.
Este avance demuestra que es posible reconstruir el metabolismo central sin comprometer la salud celular. En el futuro, estas “bacterias híbridas” podrían ser fábricas celulares ultrarrentables que produzcan biocombustibles y bioplásticos con una huella de carbono drásticamente menor.

📚 REFERENCIA BIBLIOGRÁFICA
Lin, Y.-J., Chen, H.-T., Lin, P.-Y., Lai, Y.-J., & Li, S.-Y. (2026). Coordinating Calvin Cycle and Glycolysis in Escherichia coli. ACS Synthetic Biology. https://doi.org/10.1021/acssynbio.5c00854