Un estudio de transcriptómica avanzada redefine cómo las bacterias regulan sus redes genéticas: no solo encendiendo y apagando promotores, sino “secuestrando” reguladores postranscripcionales.
La vida bacteriana es una constante batalla entre la economía energética y la supervivencia. Caulobacter crescentus, una alfaproteobacteria modelo que habita ambientes acuáticos pobres en nutrientes (oligotróficos), debe adaptar su proteoma en minutos cuando los niveles de carbono fluctúan. Un estudio reciente publicado en Nature Communications ha desentrañado un circuito regulatorio fascinante que involucra interacciones ARN-ARN dependientes de Hfq, revelando un mecanismo de “esponja” molecular esencial para la transición metabólica.
🔬 La Metodología: RIL-seq para mapear el interactoma
Para comprender las redes regulatorias, los investigadores de la Universidad de Jena no se limitaron a una RNA-seq tradicional. Utilizaron RIL-seq (RNA interaction by ligation and sequencing).

- ¿Cómo funciona? Co-inmunoprecipitaron la proteína chaperona Hfq (que estabiliza interacciones entre ARNs bacterianos) junto con los ARNs unidos a ella. Luego, ligaron los extremos de los ARNs que estaban cerca (interactuando) y secuenciaron las quimeras resultantes.
- El Hallazgo: Recuperaron miles de quimeras ARN-ARN, revelando una red oculta. Lo más sorprendente fue que el sRNA (small RNA) conocido como CrfA no se unía a mRNAs como se creía, sino a otros sRNAs.


🧩 El Circuito “Banquete vs. Hambruna”
El estudio describe un sistema de regulación post-transcripcional jerárquico compuesto por dos actores principales:
1. Los Represores: La familia SisA-D (Feast)
En condiciones de abundancia de nutrientes (glucosa/xilosa), Caulobacter expresa constitutivamente cuatro sRNAs homólogos llamados SisA, SisB, SisC y SisD (familia R8).

- Función: Estos sRNAs se unen a la región 5′ UTR de mRNAs específicos mediante un motivo conservado de 10 nucleótidos, bloqueando su traducción o promoviendo su degradación.
- Blancos: Reprimen genes costosos que no son necesarios en abundancia, como los receptores dependientes de TonB (TBDRs) y enzimas para metabolizar fuentes de carbono complejas o exóticas.
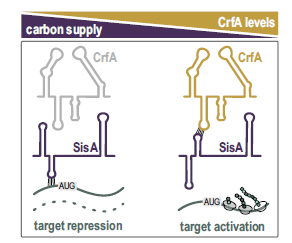
2. La Esponja: CrfA (Famine)
Cuando hay inanición de carbono, la célula induce fuertemente la transcripción del sRNA CrfA.
- Mecanismo de Acción (Sponge): CrfA no regula genes directamente. En su lugar, contiene una secuencia que mimetiza el sitio de unión de los mRNAs blanco. CrfA actúa como un señuelo o “esponja”, uniéndose a SisA (y sus hermanos) con alta afinidad gracias a la chaperona Hfq.

- Consecuencia Molecular: Al secuestrar a SisA, CrfA no solo impide que este reprima a sus blancos, sino que promueve la degradación rápida de SisA. Esto limpia el citoplasma de represores en cuestión de minutos.

⚙️ Lógica Biológica: ¿Por qué usar una esponja?
Uno podría preguntarse: ¿Por qué la bacteria no simplemente deja de transcribir SisA?
Para un estudiante universitario, la respuesta radica en la cinética enzimática y la respuesta al estrés:
- Velocidad: Detener la transcripción es lento; los sRNAs ya sintetizados seguirían reprimiendo los genes metabólicos necesarios para sobrevivir. Una esponja de ARN elimina la actividad del represor instantáneamente.
- Histéresis y Umbrales: Este mecanismo permite establecer umbrales precisos. Solo cuando el estrés es suficiente para producir suficiente CrfA como para titular (neutralizar) a todo el SisA, se activa la respuesta metabólica.
- Eficiencia Energética: Permite mantener apagados genes de transporte costosos (TBDRs) hasta que sean estrictamente necesarios.
📉 Impacto Fenotípico
El estudio demostró que los mutantes (sin la esponja) tienen graves defectos de crecimiento cuando se les somete a ciclos de hambruna y realimentación. Al no poder eliminar a SisA rápidamente, la bacteria no logra expresar a tiempo los transportadores necesarios para aprovechar los nuevos nutrientes, quedando en una desventaja competitiva letal en la naturaleza.
📜 Conclusión
Este trabajo corrige la literatura previa (que asumía que CrfA actuaba sobre mRNAs) y establece a Caulobacter como un modelo para estudiar la competencia de ARN en procariotas. Nos muestra que las bacterias emplean estrategias de regulación tan sofisticadas como los miARNs y “cebos” de ARN (ceRNA) que observamos en células eucariotas.

📖 Referencia Completa:
Vogt, L. N., Velasco Gomariz, M., Siemers, M., Papenfort, K., & Fröhlich, K. S. (2025). An RNA sponge directs the transition from feast to famine in Caulobacter crescentus. Nature Communications, 16:9478. https://doi.org/10.1038/s41467-025-65274-1