El Secreto de la Vida en Suspenso
En el reino animal, la capacidad de entrar en estados de animación suspendida o diapausia es una estrategia de supervivencia extraordinaria. Organismos como el gusano nematodo Caenorhabditis elegans pueden detener su desarrollo y envejecimiento durante meses en una forma de “hibernación” llamada diapausa reproductiva del adulto (ARD), para luego “despertar”, regenerarse y reproducirse como si el tiempo no hubiera pasado. ¿Cómo logran esta increíble hazaña de resiliencia y longevidad? ¿Qué mecanismos moleculares protegen a sus células, especialmente a las células madre, de la degradación y el envejecimiento durante este período? Un estudio fundamental publicado en la prestigiosa revista Nature Aging por Tim J. Nonninger, Adam Antebi y un equipo internacional de colaboradores, ha identificado un eje de señalización molecular clave, TFEB-TGFβ, que actúa como un interruptor maestro, controlando la diapausa, la resiliencia de las células madre y protegiendo al organismo de un estado similar a la senescencia.
El Modelo: C. elegans y su “Pausa” Anti-Envejecimiento
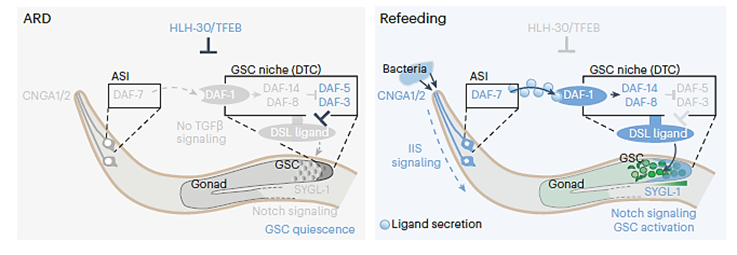
C. elegans es un modelo poderoso para estudiar el envejecimiento. En respuesta a la escasez de alimentos, los gusanos adultos pueden entrar en ARD, un estado en el que viven mucho más tiempo de lo normal. El equipo de investigación se centró en el regulador maestro de la ARD, un factor de transcripción llamado HLH-30/TFEB (TFEB es su homólogo en mamíferos). Descubrieron que cuando HLH-30 está mutado y no funciona correctamente, el gusano no solo muere rápidamente durante la ARD, sino que sus células madre germinales (las que dan origen a óvulos y esperma) entran en un estado de senescencia, un estado de “envejecimiento celular” irreversible.

Los Sellos de la Senescencia en Células Madre
Los gusanos mutantes para hlh-30 mostraban todos los signos clásicos de la senescencia celular en sus células madre germinales:
- Daño en el ADN: Acumulación de roturas en el ADN.
- Arresto del Ciclo Celular: Incapacidad de las células para dividirse y proliferar.
- Disfunción Mitocondrial: Las mitocondrias (las centrales energéticas de la célula) se veían anormales y producían más especies reactivas de oxígeno (estrés oxidativo).
- Expansión del Nucléolo y Envejecimiento Acelerado: Presentaban nucléolos agrandados y otros marcadores de envejecimiento a nivel de todo el organismo.

Esto demostró que HLH-30/TFEB es esencial para proteger a las células madre de caer en un estado de senescencia durante la diapausa. Pero ¿cómo lo hace?
La Vía TGFβ: El Eje de Control
Para encontrar los mecanismos que operan junto a TFEB, los investigadores realizaron un cribado genético, buscando mutaciones en otros genes que pudieran “rescatar” a los gusanos mutantes para hlh-30. Sorprendentemente, encontraron que desactivar la vía de señalización del factor de crecimiento transformante beta (TGFβ) restauraba la longevidad y la resiliencia de las células madre en estos mutantes.

Esto reveló la existencia de un eje regulador crucial: TFEB-TGFβ.
- En condiciones de ayuno (diapausia): TFEB se activa y suprime la señalización de TGFβ. Esto es crucial para mantener la quiescencia y proteger a las células madre.
- En mutantes hlh-30: Sin TFEB funcional, la vía TGFβ no se suprime adecuadamente durante la diapausa. Esta señalización de crecimiento “fuera de lugar” en un momento de escasez de nutrientes es lo que empuja a las células madre hacia la senescencia y el colapso.

Esencialmente, TFEB actúa como un coordinador maestro que alinea el estado nutricional del organismo con las vías de señalización de crecimiento, asegurando que las células solo crezcan y se dividan cuando hay recursos disponibles y que permanezcan en un estado protegido de quiescencia cuando no los hay. Una desalineación de este sistema conduce directamente al envejecimiento celular.
De Gusanos a Mamíferos: Un Mecanismo Conservado
Lo más emocionante de este descubrimiento es su relevancia para los mamíferos. Los investigadores demostraron que el papel de TFEB en la protección contra la senescencia está conservado evolutivamente:
- Diapausa Embrionaria de Ratón: TFEB también es crucial para la supervivencia de las células madre embrionarias de ratón durante la diapausa.
- Células de Cáncer Humano: Las células de melanoma humano pueden entrar en un estado de “diapausia” para resistir la quimioterapia. El estudio demostró que la inactivación de TFEB en estas células cancerosas “durmientes” las hacía vulnerables y reducía su supervivencia, mientras que no afectaba a las células proliferantes.
Implicaciones: Entendiendo la Senescencia y Combatiendo el Cáncer y el Envejecimiento
Este estudio tiene implicaciones profundas y de gran alcance:
- Nuevo Modelo para la Senescencia: La diapausa en C. elegans emerge como un modelo poderoso para estudiar la senescencia in vivo y cómo se puede prevenir o revertir, especialmente en células madre.
- Una Causa Fundamental de la Senescencia: Sugiere que el envejecimiento celular puede surgir de una desalineación entre la percepción de nutrientes y las vías de señalización de crecimiento, un concepto que podría ser aplicable a muchos contextos de envejecimiento.
- Nueva Estrategia Contra el Cáncer: Apuntar a TFEB podría ser una estrategia terapéutica para eliminar las células cancerosas “durmientes” que causan recaídas después de la quimioterapia. Al inactivar TFEB, se podría empujar a estas células resistentes a la muerte.
- Envejecimiento Saludable: Comprender cómo el eje TFEB-TGFβ mantiene la resiliencia de las células madre podría abrir nuevas vías para promover un envejecimiento más saludable y mantener la homeostasis de los tejidos.

Conclusión: Un Circuito Ancestral para la Juventud Celular
El trabajo de Nonninger, Antebi y su equipo ha desvelado un circuito regulador primordial y conservado evolutivamente, el eje TFEB-TGFβ, que orquesta la capacidad de un organismo para entrar en un estado de resiliencia y proteger a sus células madre del envejecimiento. Al vincular directamente la percepción de nutrientes con las vías de crecimiento, este mecanismo se erige como un guardián fundamental de la longevidad celular y del organismo. Este descubrimiento no solo nos proporciona una visión sin precedentes de los secretos de la diapausa, sino que también nos ofrece un nuevo y poderoso modelo para estudiar la senescencia y, lo que es más importante, nos brinda nuevas y prometedoras dianas terapéuticas para combatir tanto el envejecimiento como la persistencia del cáncer.
Referencia del Artículo:
Nonninger, T. J., Mak, J., Gerisch, B., Ramponi, V., Kawamura, K., Ripa, R., … & Antebi, A. (2025). A TFEB-TGFβ axis systemically regulates diapause, stem cell resilience and protects against a senescence-like state. Nature Aging. https://doi.org/10.1038/s43587-025-00911-4
(Publicado online; el volumen y número de página final pueden variar).