En Pocas Palabras:
La terapia génica utiliza virus adeno-asociados (AAV) como “taxis” para entregar genes correctivos a las células. El éxito de esta terapia depende de un receptor principal en la superficie celular, llamado AAVR, al que se unen la mayoría de los AAVs para poder entrar. Sin embargo, usar altas dosis de estos vectores puede causar toxicidad. Un nuevo estudio ha descubierto un segundo receptor alternativo, AAVR2, que ciertos serotipos de AAV (como AAV8, AAV11 y AAV12) pueden usar como una “puerta trasera” para entrar a las células. Este hallazgo no solo profundiza nuestro conocimiento de la biología de los AAV, sino que abre la puerta a soluciones clínicas innovadoras: al sobreexpresar una versión mínima y funcional de AAVR2 en los tejidos diana, se podría aumentar la eficiencia de la terapia génica, permitiendo usar dosis mucho más bajas y seguras de los vectores virales.

El Auge y los Desafíos de la Terapia Génica con AAV
La terapia génica ha pasado de ser una promesa futurista a una realidad clínica que está transformando la medicina. En el centro de muchos de estos avances se encuentran los vectores de virus adeno-asociados (AAV), pequeñas cápsides virales modificadas que actúan como vehículos de alta precisión para entregar material genético correctivo a las células de pacientes con enfermedades como la hemofilia, la atrofia muscular espinal o ciertos tipos de ceguera. Sin embargo, a pesar de su éxito, uno de los mayores desafíos sigue siendo la necesidad de usar dosis muy altas de estos vectores para lograr un efecto terapéutico, lo que puede llevar a toxicidad y efectos secundarios graves. Un nuevo y revolucionario estudio publicado en la revista Cell por Bijay P. Dhungel, John E.J. Rasko y un equipo internacional de colaboradores, ha identificado un receptor alternativo para estos virus, un hallazgo que no solo cambia nuestra comprensión fundamental de cómo los AAV interactúan con nuestras células, sino que también ofrece una solución clínicamente aplicable para hacer la terapia génica mucho más segura y eficiente.
La “Llave Maestra” Conocida: El Receptor AAVR
Hasta ahora, se sabía que la mayoría de los serotipos de AAV (las diferentes “versiones” del virus) dependen de un receptor principal en la superficie celular para poder entrar e infectar a las células. Este receptor, conocido como AAVR, actúa como una especie de “cerradura” universal a la que se unen múltiples AAVs. La interacción AAV-AAVR es el primer paso crucial para una terapia génica exitosa. Sin embargo, la biología viral rara vez es tan simple, y la existencia de vías de entrada independientes de AAVR era una posibilidad que intrigaba a los científicos.

El Descubrimiento: AAVR2, una “Puerta Trasera” Inesperada
Utilizando un cribado genómico de activación por CRISPR en células humanas que carecían del receptor AAVR, los investigadores buscaron genes que, al ser activados, pudieran rescatar la capacidad del AAV8 (un serotipo muy utilizado en clínica) para entrar en las células. El resultado fue inequívoco: identificaron a la carboxipeptidasa D (CPD), a la que rebautizaron como AAVR2, como un nuevo receptor funcional para los AAV.
Los hallazgos clave sobre AAVR2 fueron:
- Selectividad de Serotipos: AAVR2 no es universal. Su función es específica para ciertos serotipos, principalmente los del clado E (como AAV8, AAVrh10), y es el receptor exclusivo para los serotipos AAV11 y AAV12. Esto significa que estos dos últimos virus utilizan únicamente esta “puerta trasera” para entrar, siendo completamente independientes de AAVR.
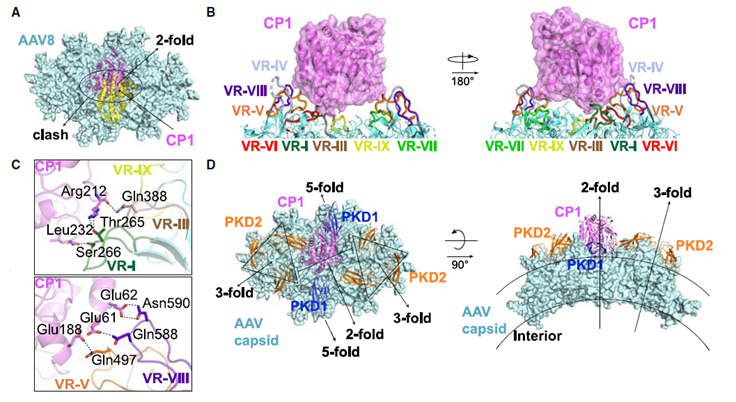
- Mecanismo de Unión Directo: Mediante técnicas de criomicroscopía electrónica (cryo-EM), el equipo resolvió la estructura tridimensional del complejo AAV8-AAVR2 a una resolución de 2.32 Å. Demostraron que AAV8 se une directamente al primer dominio tipo carboxipeptidasa (CP1) de AAVR2, y que esta interacción es mediada por una región variable específica (VR-VIII) en la cápside del AAV8. Curiosamente, el modo de unión a AAVR2 es estructuralmente distinto a cómo otros AAVs se unen a AAVR, explicando la selectividad.
- La Función se Puede Transferir: Demostraron que la capacidad de usar AAVR2 es transferible. Al modificar un AAV (AAV2) que normalmente no usa AAVR2 e insertarle la región VR-VIII del AAV8, lograron que este virus quimérico pudiera usar AAVR2 para entrar en las células.
De la Biología Fundamental a la Aplicación Clínica: “miniAAVR2”
El hallazgo más trascendental del estudio es cómo esta nueva conocimiento puede traducirse en una mejora tangible para la terapia génica. Los investigadores diseñaron una versión mínima y funcional de AAVR2, a la que llamaron “miniAAVR2”.
La idea es simple pero poderosa: si se puede aumentar la cantidad de “puertas de entrada” (AAVR2) en el tejido diana, se necesitará una dosis mucho menor del “taxi” viral (el vector AAV) para lograr el mismo efecto terapéutico.
Y funcionó a la perfección. En modelos de ratón, la coadministración de un vector AAV que expresaba “miniAAVR2” junto con el vector terapéutico AAV8 aumentó significativamente la eficiencia de la terapia génica en el hígado y el músculo. Esto permitió lograr el mismo nivel de entrega de genes con dosis mucho más bajas, lo que podría reducir drásticamente los riesgos de toxicidad asociados a las altas dosis de vectores que se usan actualmente en la clínica.

Implicaciones y Futuro de la Terapia Génica
Este estudio representa un avance fundamental con implicaciones de gran alcance:
- Comprensión de la Biología Viral: Cambia el dogma de que AAVR es el único receptor principal y revela una nueva capa de complejidad y especificidad en las interacciones AAV-huésped.
- Mejora de la Seguridad y Eficacia: La estrategia de sobreexpresión de “miniAAVR2” es una solución clínicamente desplegable que podría hacer las terapias génicas existentes y futuras más seguras y eficientes.
- Diseño de Nuevos Vectores: El conocimiento de los residuos exactos que median la interacción AAV8-AAVR2 permitirá el bioingeniería de nuevas cápsides virales con tropismo y afinidad controlados, diseñadas a medida para interactuar con AAVR, AAVR2, o ambos.
- Expansión de la Terapia Génica: Al mejorar el perfil de seguridad, esta estrategia podría expandir el uso de la terapia génica con AAV a más enfermedades y a un mayor número de pacientes.

Conclusión: Una Nueva Llave para Abrir las Puertas de la Terapia Génica
El descubrimiento del receptor alternativo AAVR2 por Dhungel, Rasko y su equipo es un hito que redefine el mapa de la entrada celular de los AAV. Más allá del avance en la biología fundamental, la demostración de que una versión mínima de este nuevo receptor puede potenciar drásticamente la terapia in vivo ofrece una solución elegante y poderosa a uno de los mayores obstáculos de la terapia génica: la toxicidad relacionada con la dosis. Este trabajo no solo nos proporciona una nueva “llave”, sino que nos enseña que, a veces, para mejorar una terapia, la solución no es enviar más “taxis”, sino construir más “puertas de entrada” en el destino correcto.
Referencia del Artículo:
Dhungel, B. P., Xu, H., Nagarajah, R., Su, X.-d., Bailey, C. G., & Rasko, J. E. J. (2025). An alternate receptor for adeno-associated viruses. Cell, 188, 1–12. https://doi.org/10.1016/j.cell.2025.06.026
(Publicado online; la paginación final y la lista completa de autores pueden variar en la versión final).