En Pocas Palabras:
Cuando te quemas con el sol, la piel se enrojece, inflama y duele. Tradicionalmente, hemos culpado de esta reacción al daño que la radiación UVB causa directamente en el ADN de nuestras células. Sin embargo, un nuevo y revolucionario estudio demuestra que esta no es la historia completa, y ni siquiera la principal al principio. La reacción aguda de la quemadura solar (inflamación, muerte celular, engrosamiento de la piel) no es causada por el daño al ADN nuclear, sino por el daño que los rayos UV infligen al ARN mensajero (ARNm) en el citoplasma. Este daño provoca que los ribosomas (las fábricas de proteínas de la célula) se “atasquen”, generando un “estrés ribotóxico”. Una proteína sensora clave, ZAKα, detecta este caos en la producción de proteínas y desencadena una rápida cascada de inflamación y muerte celular que conocemos como quemadura solar. Este hallazgo cambia fundamentalmente nuestra comprensión de la biología de la piel y abre nuevas vías para tratar las quemaduras solares y otras enfermedades inflamatorias de la piel.
El Antiguo Misterio de la Quemadura Solar
Todos hemos experimentado, en mayor o menor medida, los efectos de una exposición excesiva al sol: enrojecimiento, dolor, inflamación y, finalmente, descamación de la piel. Durante décadas, el dogma científico ha sido claro: la radiación ultravioleta B (UVB) del sol es dañina porque causa mutaciones y roturas en el ADN de las células de nuestra piel, los queratinocitos. Se creía que la respuesta del cuerpo a este daño genético era la principal causa de la inflamación y la muerte celular que caracterizan a una quemadura solar. Sin embargo, un nuevo y elegante estudio publicado en la prestigiosa revista Molecular Cell por Anna Constance Vind, Simon Bekker-Jensen y un equipo internacional, pone este dogma patas arriba, revelando que el principal culpable de la reacción aguda de la quemadura solar no es el núcleo y su ADN, sino la maquinaria celular del citoplasma.

El Verdadero Origen del Problema: El Estrés Ribotóxico
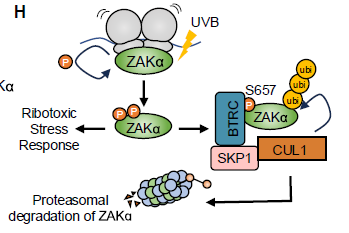
Los investigadores descubrieron que la radiación UVB, además de dañar el ADN, también causa estragos en el ARN mensajero (ARNm), la molécula que lleva las instrucciones del ADN a los ribosomas para fabricar proteínas. Cuando los ribosomas intentan “leer” un ARNm dañado por los rayos UV, se atascan, chocan entre sí y provocan un “embotellamiento” en la línea de producción de proteínas. Este fenómeno se conoce como respuesta al estrés ribotóxico (RSR).
El estudio identifica a una proteína quinasa clave, ZAKα (MAP3K20), como el sensor principal de este caos. ZAKα, que reside en el citoplasma, detecta el “atasco” de los ribosomas y, al activarse, desencadena una potente cascada de señalización a través de otras proteínas (las quinasas p38 y JNK).


La Cascada de Reacciones: Muerte Celular e Inflamación
La activación de la vía ZAKα-p38/JNK tiene consecuencias dramáticas y rápidas para la piel:
- Muerte Celular Programada: Se activan dos tipos de muerte celular para eliminar los queratinocitos dañados:
- Piroptosis (vía p38): Una forma de muerte celular altamente inflamatoria, donde la célula literalmente “estalla”, liberando citoquinas y quimioquinas que atraen a las células inmunes.
- Apoptosis (vía JNK): Una forma más “ordenada” de suicidio celular.
- Inflamación y Engrosamiento de la Piel: La liberación de moléculas inflamatorias y la muerte celular masiva provocan la infiltración de células inmunes (como neutrófilos y monocitos) en la dermis, causando la inflamación y el enrojecimiento característicos. Como respuesta compensatoria, los queratinocitos supervivientes comienzan a proliferar, lo que lleva al engrosamiento de la epidermis.
La Evidencia Contundente: Los Ratones “a Prueba de Sol”
Para probar su hipótesis, el equipo utilizó un modelo de ratón genéticamente modificado que carecía del gen Zak (ratones ZAK-/-). Los resultados fueron asombrosos:
- Cuando se irradiaba con UVB la piel de los ratones normales (WT), se observaba la rápida activación de p38 y JNK, muerte celular, infiltración de células inmunes y engrosamiento de la piel.
- En los ratones ZAK-/-, ¡todas estas respuestas agudas estaban significativamente atenuadas o completamente ausentes! Estos ratones estaban, en gran medida, protegidos de los efectos inmediatos de la quemadura solar.
Para confirmar que el estrés ribotóxico era suficiente para causar estos efectos, aplicaron tópicamente en las orejas de los ratones una sustancia llamada anisomicina, que causa estrés ribotóxico sin dañar el ADN. Los ratones normales desarrollaron inflamación y engrosamiento, mientras que los ratones ZAK-/- no lo hicieron. Esto demuestra de manera concluyente que es la vía de la RSR, y no la respuesta al daño del ADN, la que orquesta la respuesta aguda a la quemadura solar.

Implicaciones y Futuro: Nuevas Dianas Terapéuticas
Este cambio de paradigma tiene implicaciones muy importantes:
- Nueva Comprensión de la Biología de la Piel: Redefine la quemadura solar como una respuesta rápida y citoplasmática al daño del ARNm, relegando la respuesta al daño del ADN a un papel más tardío, probablemente más relacionado con la reparación a largo plazo y el riesgo de cáncer de piel.
- Nuevas Terapias para Quemaduras Solares: En lugar de tratar solo los síntomas (como el dolor y la inflamación), se podrían desarrollar cremas o lociones con inhibidores de ZAKα o de las quinasas p38/JNK. Aplicados después de la exposición al sol, estos podrían prevenir o mitigar la reacción de la quemadura solar en su origen.
- Conexiones con Otras Enfermedades de la Piel: Dado que esta vía está fuertemente ligada a la inflamación, podría estar implicada en otras enfermedades inflamatorias de la piel como la psoriasis o la dermatitis atópica, abriendo nuevas vías para su tratamiento.
Conclusión: Una Respuesta Elegante a un Problema Cotidiano
El estudio de Vind y colaboradores es un ejemplo brillante de cómo la investigación fundamental puede cambiar nuestra comprensión de un fenómeno cotidiano. Al desplazar el foco del daño nuclear del ADN al estrés citoplasmático de los ribosomas, han identificado a ZAKα y la respuesta al estrés ribotóxico como los verdaderos directores de orquesta de la respuesta aguda de la piel al sol. Este descubrimiento no solo es elegante desde el punto de vista científico, sino que también es inmensamente prometedor, ya que nos ofrece nuevas y específicas dianas moleculares para desarrollar tratamientos más eficaces contra las quemaduras solares y, potencialmente, otras afecciones inflamatorias de la piel.
Referencia del Artículo:
Vind, A. C., Wu, Z., Firdaus, M. J., Snieckute, G., Toh, G. A., Jessen, M., … & Bekker-Jensen, S. (2024). The ribotoxic stress response drives acute inflammation, cell death, and epidermal thickening in UV-irradiated skin in vivo. Molecular Cell, 84(24), 4774-4789. https://doi.org/10.1016/j.molcel.2024.10.044