En Pocas Palabras:
Candida albicans es un hongo común que normalmente vive en nosotros sin causar problemas. Para volverse patógeno, tradicionalmente se pensaba que necesitaba formar filamentos (hifas) y producir toxinas. Sin embargo, muchas cepas aisladas de pacientes con infecciones graves parecen inofensivas en el laboratorio, un enigma para la ciencia. Un nuevo estudio ha descubierto el factor clave que faltaba en los experimentos: la albúmina, la proteína más abundante en la sangre humana. La presencia de albúmina “despierta” una vía de patogenicidad alternativa en Candida. El hongo reprograma su metabolismo, aumenta la formación de biopelículas y comienza a producir un lípido llamado 13-HODE, que es tóxico para las células humanas. Este mecanismo, independiente de los factores de virulencia clásicos, explica cómo cepas aparentemente “débiles” pueden causar enfermedades graves una vez que están dentro de nuestro cuerpo.
El Enigma de la Virulencia de Candida albicans
Candida albicans es un hongo oportunista que forma parte de nuestro microbioma normal, colonizando a la mayoría de la población sin causar daño. Sin embargo, cuando las defensas del huésped se debilitan, puede causar infecciones que van desde las superficiales (como la candidiasis oral o vaginal) hasta las sistémicas y potencialmente mortales. El dogma científico ha sostenido durante mucho tiempo que la capacidad de Candida para causar enfermedad depende de un arsenal de “armas” bien conocidas: la capacidad de adherirse a las células, formar filamentos invasivos llamados hifas y producir una potente toxina llamada candidalisina. Pero aquí reside un enigma: muchas cepas de Candida aisladas de pacientes con infecciones graves parecen sorprendentemente “inofensivas” cuando se estudian en el laboratorio (ex vivo), careciendo de estas características. Un nuevo y revelador estudio publicado en Nature Communications por Sophia U. J. Hitzler, Mark S. Gresnigt y un equipo internacional de investigadores, ha resuelto este misterio identificando un factor del huésped, la albúmina, como el interruptor que activa una vía de patogenicidad completamente alternativa.

La Albúmina: Más que una Simple Proteína Sanguínea
La albúmina es la proteína más abundante en el plasma sanguíneo humano. Su función principal es mantener la presión osmótica y transportar diversas moléculas. Los investigadores plantearon la hipótesis de que las condiciones del laboratorio carecen de factores clave presentes en el cuerpo humano (in vivo) que podrían “despertar” la virulencia de estas cepas aparentemente avirulentas. Pusieron su atención en la albúmina.
Al añadir albúmina a sus cultivos in vitro, los resultados fueron sorprendentes:
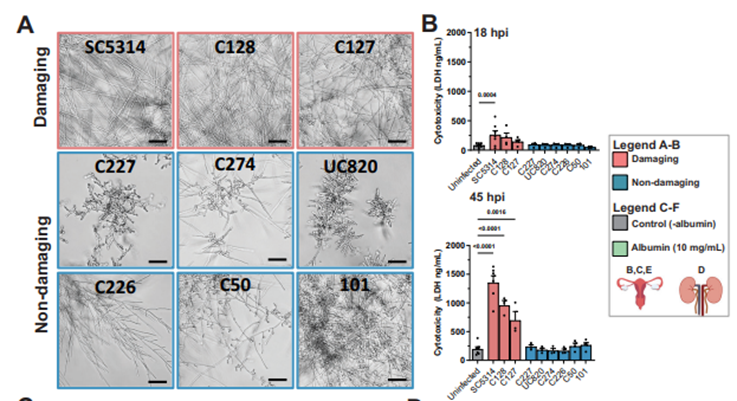
- “Despertar” de la Virulencia: Cepas de Candida que eran no dañinas y no filamentosas se volvieron altamente citotóxicas para las células epiteliales humanas en presencia de albúmina. Su capacidad para dañar y matar las células huésped se restauró por completo.
- Mecanismo Independiente de las Armas Clásicas: Aún más sorprendente, mutantes de Candida que carecían de los factores de virulencia canónicos (incapaces de formar hifas, de adherirse o de producir la toxina candidalisina) también se volvieron citotóxicos en presencia de albúmina. Esto demostró que la albúmina estaba activando una vía de patogenicidad completamente nueva e independiente de los mecanismos conocidos.

Reprogramación Metabólica y una Nueva Toxina Lipídica
Para entender cómo la albúmina lograba este efecto, los investigadores realizaron análisis transcriptómicos y metabolómicos completos, que revelaron una reprogramación masiva del hongo:
- Cambio Metabólico: En presencia de albúmina, Candida alteraba drásticamente su metabolismo, desviándose de la glicólisis hacia la utilización de lípidos y aminoácidos, y aumentando su respiración.
- Aumento de Biopelículas: La reprogramación incluía un aumento en la formación de biopelículas, lo que ayuda al hongo a establecerse y persistir en la infección.
- Identificación del Arma Secreta: 13-HODE: El análisis del “exometaboloma” (las moléculas que el hongo secreta) reveló el hallazgo clave: en presencia de albúmina, Candida comenzaba a producir y liberar grandes cantidades de un oxilípido (un ácido graso oxidado) llamado ácido 13-hidroxioctadecadienoico (13-HODE).
- 13-HODE es Citotóxico: Cuando los investigadores añadieron 13-HODE purificado a las células epiteliales, este compuesto por sí solo fue capaz de inducir la citotoxicidad, confirmando que era el principal ejecutor de esta nueva vía de patogenicidad.

Esencialmente, la albúmina no solo actúa como una señal, sino que también es utilizada por el hongo como una fuente de nutrientes (ácidos grasos) que son metabolizados para producir esta molécula tóxica.
Implicaciones: Entendiendo la Infección y Mejorando los Modelos
Este descubrimiento tiene implicaciones profundas para la microbiología médica y el estudio de las enfermedades infecciosas:
- Redefinición de la Virulencia de Candida: Demuestra que la virulencia de Candida albicans es mucho más plástica y contextual de lo que se pensaba. El hongo tiene un “Plan B” que puede activar cuando se encuentra en el entorno rico en albúmina del torrente sanguíneo o de los tejidos profundos.
- Resolución de una Paradoja Clínica: Explica por qué muchas cepas clínicas parecen avirulentas ex vivo: los modelos de laboratorio estándar simplemente carecen de las señales del huésped (como la albúmina) necesarias para activar todos sus programas de patogenicidad.
- Mejora de los Modelos de Infección: Subraya la necesidad crítica de desarrollar modelos in vitro más fisiológicamente relevantes (que incluyan componentes del huésped como la albúmina) para evaluar con mayor precisión la virulencia de los patógenos y la eficacia de los fármacos antifúngicos.
- Nuevas Dianas Terapéuticas: La vía metabólica que conduce a la producción de 13-HODE podría ser una nueva diana para el desarrollo de fármacos antifúngicos que bloqueen esta vía de patogenicidad alternativa.
Conclusión: Un Diálogo Químico entre Huésped y Patógeno
El estudio de Hitzler, Gresnigt y sus colegas es un elegante ejemplo de cómo el diálogo químico entre un patógeno y su huésped puede dictar el resultado de una infección. Al descubrir que la albúmina, una simple y abundante proteína del huésped, puede redirigir completamente el metabolismo de Candida albicans para activar una vía de ataque secreta basada en la producción del oxilípido tóxico 13-HODE, este trabajo resuelve un enigma de larga data y nos obliga a repensar nuestra definición de virulencia. Es un recordatorio crucial de que, para entender verdaderamente a los patógenos, debemos estudiarlos no de forma aislada, sino en el complejo contexto del entorno del huésped en el que han evolucionado para prosperar.
Referencia del Artículo:
Hitzler, S. U. J., Fernández-Fernández, C., Günther, K., Dietschmann, A., Hovhannisyan, H., Möslinger, A., … & Gresnigt, M. S. (2025). Host albumin redirects Candida albicans metabolism to engage an alternative pathogenicity pathway. Nature Communications, 16, 6447. https://doi.org/10.1038/s41467-025-61701-5