El Desafío de Entregar Medicamentos a su Destino
Los oligonucleótidos antisentido (ASOs) son una de las herramientas terapéuticas más prometedoras de la medicina moderna. Estas pequeñas moléculas sintéticas de ácido nucleico pueden diseñarse para unirse a un ARN específico y modificar su expresión, ofreciendo una forma de tratar enfermedades, especialmente aquellas causadas por genes “no fármaco-dirigibles” por métodos tradicionales. Sin embargo, su mayor desafío no es el diseño, sino la entrega: ¿cómo logran estas moléculas cruzar las membranas celulares y llegar a su objetivo en el citoplasma o el núcleo sin ser destruidas en el camino? Este proceso, conocido como “escape endosomal”, es notoriamente ineficiente. Un nuevo y revelador estudio publicado en Nature Communications por Liza Malong, Filip Roudnicky y un equipo internacional de investigadores de Roche y Genentech, ha utilizado una pantalla genética CRISPR/Cas9 a gran escala para identificar los guardianes moleculares que controlan el destino de los ASOs dentro de la célula, descubriendo que la clave para aumentar su eficacia podría estar en retrasar su viaje hacia el “estómago” celular, el lisosoma.

El Viaje Intracelular de un ASO: Un Camino Lleno de Peligros
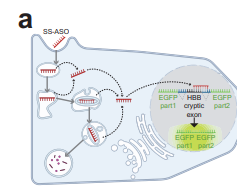
Cuando un ASO entra en una célula sin ayuda (un proceso llamado “gimnosis”), es engullido en una vesícula llamada endosoma. Este endosoma es como una estación de clasificación que madura y transporta su carga a través de la célula. La gran mayoría de los ASOs (más del 98%) nunca logran escapar de este sistema y terminan siendo transportados al lisosoma, el compartimento de degradación de la célula, donde son destruidos. Solo una pequeña fracción consigue “escapar” al citoplasma, donde puede ejercer su efecto terapéutico. Mejorar este escape es el santo grial de la terapia con ASOs.
Un Mapa Genético para el Tráfico de ASOs
Para identificar qué genes controlan este proceso, los investigadores utilizaron una ingeniosa pantalla genética basada en CRISPR/Cas9. Crearon una línea celular con un gen reportero de proteína verde fluorescente (GFP) que solo se “enciende” si un ASO logra llegar al núcleo y corregir un error de splicing. Luego, utilizaron CRISPR para inactivar, uno por uno, casi todos los genes del genoma humano. Al seleccionar las células que mostraban la mayor (o menor) fluorescencia de GFP, pudieron identificar qué genes, al ser eliminados, aumentaban o disminuían la actividad del ASO.


El Descubrimiento Clave: El Complejo AP-1 y la Interfaz Endosoma-Golgi
El resultado de la pantalla fue claro y sorprendente. Muchos de los “éxitos” más significativos, es decir, los genes que más influían en la actividad del ASO, estaban relacionados con el tráfico de vesículas entre el endosoma y el aparato de Golgi, una ruta de transporte intracelular crucial.
El protagonista principal que emergió fue el complejo adaptador de clatrina 1 (AP-1), y en particular su subunidad AP1M1.
- AP1M1 como Freno de la Actividad ASO: Cuando los investigadores eliminaron el gen AP1M1, la actividad del ASO aumentó drásticamente, tanto en líneas celulares como en modelos animales (in vivo).

- Mecanismo de Acción: La función normal de AP-1 es reciclar proteínas desde los endosomas tardíos de vuelta al aparato de Golgi. Al eliminar AP1M1, este reciclaje se interrumpe. El estudio demostró que esto no afecta a la entrada inicial de los ASOs en la célula, ni daña los lisosomas. En cambio, la eliminación de AP1M1 retrasa el transporte de la carga endosomal hacia los lisosomas.
- Más Tiempo para Escapar: Este retraso en el tráfico es la clave. Al prolongar la permanencia de los ASOs dentro del sistema endosomal, se les da más tiempo y más oportunidades para que ocurra el improbable evento del escape endosomal hacia el citoplasma. Es como si, al ralentizar la cinta transportadora que lleva al incinerador, más paquetes tuvieran la oportunidad de “caerse” y ser rescatados.
El estudio también identificó otros actores en esta ruta, como TBC1D23, una proteína que ayuda a que las vesículas derivadas de AP-1 se unan al Golgi. La eliminación de TBC1D23 tuvo el efecto contrario (disminuyó la actividad del ASO), lo que refuerza aún más la idea de que la modulación de esta interfaz endosoma-Golgi es crítica.

Implicaciones y Futuro: Hacia Terapias con ASOs Más Eficaces
Este trabajo no es solo un elegante estudio de biología celular; tiene implicaciones terapéuticas directas y muy significativas:
- Nuevas Dianas Terapéuticas: Identifica al complejo AP-1, y en particular a AP1M1, como una diana farmacológica completamente nueva para mejorar la eficacia de los ASOs. Desarrollar fármacos que inhiban transitoriamente la función de AP1M1 podría potenciar la actividad de los ASOs coadministrados.
- Un Principio Generalizable: La idea de “ralentizar” el tráfico endolisosomal para aumentar el escape podría ser una estrategia aplicable no solo a los ASOs, sino también a otras terapias basadas en ácidos nucleicos, como siRNAs y ARNm entregados a través de nanopartículas.
- Comprensión Fundamental: Proporciona el catálogo más completo hasta la fecha de los modificadores genéticos de la actividad de los ASOs, ofreciendo una hoja de ruta para futuras investigaciones sobre el tráfico intracelular de estas importantes moléculas.
- Optimización de Terapias: Al entender mejor los cuellos de botella en la entrega, se pueden diseñar ASOs de próxima generación o estrategias de co-tratamiento que sean mucho más potentes, permitiendo potencialmente el uso de dosis más bajas y reduciendo posibles efectos secundarios.


Conclusión: Navegando el Laberinto Celular para Mejorar la Medicina
El estudio de Malong, Roudnicky y sus colaboradores es una obra maestra de la genómica funcional que ilumina una de las “cajas negras” de la farmacología moderna: cómo las terapias basadas en oligonucleótidos navegan por el complejo laberinto del interior celular. Al identificar la ruta de tráfico endosoma-Golgi, y específicamente el complejo AP-1, como un punto de control crítico, han descubierto una “puerta trasera” molecular que puede ser manipulada para aumentar drásticamente la eficacia de estas terapias. Este hallazgo no solo resuelve un enigma fundamental de la biología celular, sino que también pavimenta el camino hacia una nueva generación de medicamentos basados en ASOs, más potentes y efectivos.
Referencia del Artículo:
Malong, L., Roskosch, J., Hager, C., Fortin, J.-P., Schmucki, R., Callow, M. G., … & Roudnicky, F. (2025). A CRISPR/Cas9 screen reveals proteins at the endosome-Golgi interface that modulate cellular anti-sense oligonucleotide activity. Nature Communications, 16, 5378. https://doi.org/10.1038/s41467-025-61039-y