En Pocas Palabras:
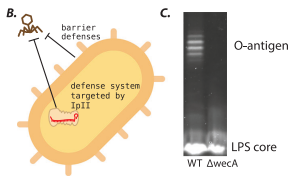
Las bacterias tienen sistemas de defensa de múltiples capas para protegerse de los virus (fagos), como un castillo con murallas exteriores y guardias interiores. Un nuevo estudio ha revelado cómo los fagos han evolucionado para superar estas defensas en una estrategia de dos pasos. Primero, utilizan pequeñas proteínas para sabotear la “muralla” exterior de la bacteria (una barrera de azúcares llamada antígeno O), lo que les permite aterrizar e inyectar su material genético. Una vez dentro, despliegan un segundo conjunto de proteínas “agentes especiales” (llamadas Ip) que se inyectan junto con el ADN viral para neutralizar a los “guardias internos” (enzimas que destruyen el ADN viral). Sorprendentemente, cada agente especial es un especialista que solo puede desactivar un tipo específico de guardia. Este descubrimiento desvela la complejidad de la carrera armamentista entre virus y bacterias y es crucial para el futuro desarrollo de la terapia con fagos para combatir infecciones resistentes a los antibióticos.
La Guerra Invisible y sus Múltiples Frentes
En el mundo microscópico se libra una batalla incesante y de consecuencias épicas: la guerra entre las bacterias y los virus que las infectan, conocidos como bacteriófagos o fagos. Esta lucha ha impulsado una carrera armamentista evolutiva, donde las bacterias han desarrollado un arsenal diverso de sistemas de defensa para protegerse, y los fagos, a su vez, han ideado ingeniosas contramedidas. Sin embargo, cómo cooperan estas defensas en bacterias “salvajes” y cómo los fagos logran superarlas sigue siendo un área de intenso estudio. Un nuevo y fascinante artículo publicado en Nature Communications por Sukrit Silas, Joseph Bondy-Denomy y un equipo de colaboradores, utiliza una innovadora plataforma de cribado funcional para, literalmente, “pelar las capas” de la inmunidad bacteriana en E. coli, revelando una sofisticada estrategia de ataque de dos pasos que los fagos utilizan para asegurar su éxito.

Capa 1: La Barrera Exterior del Antígeno O
La primera línea de defensa de muchas bacterias Gram-negativas como E. coli es su superficie celular, específicamente una capa de polisacáridos complejos llamada antígeno O. Esta capa puede actuar como una barrera física que oculta los receptores a los que los fagos necesitan unirse para poder inyectar su material genético. Es como la muralla de un castillo que impide que el enemigo se acerque a la puerta.
Utilizando un cribado a gran escala de genes accesorios de fagos, los investigadores descubrieron un conjunto de pequeñas proteínas (a las que llamaron Gnarl1, 2 y 3) que, cuando se expresaban en cepas salvajes de E. coli, las hacían repentinamente vulnerables a fagos que antes no podían infectarlas. El análisis detallado reveló que estas proteínas Gnarl modifican la estructura del antígeno O, probablemente interfiriendo con su biosíntesis. Este sabotaje de la barrera superficial crea una “brecha en la muralla”, permitiendo que los fagos puedan aterrizar y comenzar su invasión. Este hallazgo es notable porque sugiere un mecanismo de “seroconversión” mucho más extendido y simple de lo que se conocía, no requiriendo el complejo conjunto de enzimas que se creía necesario.


Capa 2: Los Guardianes Internos y sus Inhibidores Específicos
Una vez que la barrera del antígeno O es superada, el fago se enfrenta a una segunda línea de defensa: las enzimas de restricción (REs) de Tipo IV. Estos son “guardianes” moleculares dentro de la célula que patrullan en busca de ADN viral y lo destruyen. El estudio se centró en una familia particular de estas enzimas, conocidas como GmrSD, que son comunes en E. coli.

Al “pelar” la primera capa de defensa (ya sea genéticamente, eliminando el antígeno O, o funcionalmente, usando las proteínas Gnarl), los investigadores pudieron observar esta segunda capa de inmunidad en acción. Y, lo que es más importante, descubrieron las contramedidas del fago:
- El fago T4, un virus bien estudiado, inyecta junto con su ADN un conjunto de “proteínas internas” (Ip1, Ip2, Ip3) que actúan como “fuerzas especiales” para neutralizar a los guardianes.
- El estudio demostró, por primera vez, la función de Ip2 e Ip3. Descubrieron que estas proteínas son inhibidores altamente específicos de diferentes variantes de las enzimas GmrSD encontradas en distintas cepas de E. coli.
- La especificidad es asombrosa: Ip1 inhibe un tipo de GmrSD, Ip2 inhibe otro, y Ip3 un tercero, sin que haya un cruce funcional entre ellos. Es como tener una llave maestra diferente para cada cerradura específica.

Una Carrera Armamentista de Alta Especificidad
Este descubrimiento pinta un cuadro fascinante de la coevolución virus-bacteria. La inmensa variabilidad y diversidad de los sistemas de defensa GmrSD en las bacterias salvajes ha impulsado la evolución de un arsenal igualmente diverso y específico de inhibidores (las proteínas Ip) en los fagos. Un solo fago como el T4 necesita llevar consigo múltiples inhibidores diferentes para poder enfrentarse con éxito a la variedad de defensas que podría encontrar en diferentes cepas de E. coli.
Implicaciones y Futuro: Hacia una Terapia con Fagos Más Inteligente
Este trabajo tiene implicaciones profundas y de gran alcance, especialmente para el campo emergente de la terapia con fagos, que busca utilizar estos virus para tratar infecciones bacterianas resistentes a los antibióticos:
- La Importancia de las Defensas de Superficie: Demuestra que las barreras superficiales como el antígeno O son un obstáculo primordial que a menudo puede “ocultar” la existencia de otras defensas internas. Para que la terapia con fagos sea efectiva, primero hay que asegurar que el fago pueda “aterrizar”.
- Hacia una Selección Racional de Fagos: En lugar de un enfoque de “ensayo y error”, este conocimiento permite una selección o ingeniería más racional de los fagos. Para tratar una infección, se podría secuenciar la bacteria para identificar su arsenal de defensa (antígeno O, GmrSDs, etc.) y luego seleccionar o diseñar un fago que porte el conjunto correcto de “llaves maestras” (Gnarls, Ips) para superar esas defensas específicas.
- Cócteles de Fagos y Proteínas: Se podrían diseñar “cócteles” terapéuticos que no solo incluyan fagos, sino también las propias proteínas Gnarl para “abrir la puerta” y hacer que las bacterias sean susceptibles a fagos que de otro modo no podrían infectarlas.
Conclusión: Desvelando las Estrategias de la Guerra Eterna
El estudio de Silas, Bondy-Denomy y sus colaboradores es una obra maestra de la genómica funcional que nos ofrece una visión sin precedentes de las complejas estrategias de ataque y defensa en el mundo microbiano. Al “pelar” sistemáticamente las capas de la inmunidad bacteriana, se ha revelado que la victoria en esta guerra eterna no depende de una sola arma, sino de un arsenal de herramientas altamente especializadas y desplegadas en un orden preciso. Este conocimiento es fundamental no solo para entender la evolución, sino también para desarrollar la próxima generación de terapias antimicrobianas que podrían salvarnos en la era de la resistencia a los antibióticos.
Referencia del Artículo:
Silas, S., Carion, H., Makarova, K. S., Sanchez Godinez, D., Haniyur, S., Volino, L., … & Bondy-Denomy, J. (2025). Anti-restriction functions of injected phage proteins revealed by peeling back layers of bacterial immunity. Nature Communications, 16, 7828. https://doi.org/10.1038/s41467-025-63056-3