En el vasto y fascinante universo que habita dentro de cada una de nuestras células, una danza incesante y meticulosamente coreografiada de moléculas define la vida misma. Entre los actores principales de este ballet molecular, los lípidos emergen como verdaderos camaleones, no solo conformando la estructura esencial de nuestras membranas celulares, sino también desempeñando papeles cruciales como fuentes de energía, mensajeros celulares y bloques constructores de diversas biomoléculas. Sin embargo, a pesar de su ubicuidad e importancia, el estudio detallado de cómo se mueven estos lípidos —cómo se transportan de un compartimento celular a otro— ha permanecido durante mucho tiempo envuelto en el misterio, limitado por las herramientas de observación disponibles. La comprensión de este tráfico, fundamental para mantener la homeostasis celular y la función adecuada de los órganos, es un desafío de proporciones colosales en el campo de la biología molecular.
Durante décadas, la visión predominante sobre el transporte de lípidos en las células se ha centrado en las vesículas, pequeñas burbujas membranosas que se desprenden de un orgánulo, viajan a través del citoplasma y se fusionan con otro, entregando su carga lipídica. Este proceso de “tráfico vesicular” es sin duda crucial para muchas funciones celulares, pero la comunidad científica ha intuido que no es la única vía, ni quizás la más dominante, para todos los tipos de lípidos. La complejidad radica en que cada orgánulo celular posee una composición lipídica única, una firma molecular distintiva que debe mantenerse activamente para que cada compartimento realice sus funciones específicas. Imaginen una ciudad donde cada edificio necesita un tipo muy particular de ladrillo y los camiones de reparto no siempre son la opción más eficiente o específica para llevar cada ladrillo al lugar exacto. Así, la pregunta de cómo las células logran esta asombrosa especificidad y rapidez en el reparto de lípidos ha sido una incógnita persistente, una pieza clave que faltaba en el rompecabezas de la fisiología celular.
Es en este contexto de desafíos y preguntas fundamentales donde irrumpe un avance científico monumental, publicado recientemente en la prestigiosa revista Nature. Un equipo internacional de investigadores, liderado por José M. Iglesias-Artola, K. Böhlig y K. Schuhmann, entre otros, ha logrado lo impensable: desarrollar una técnica innovadora que permite visualizar y cuantificar el transporte de especies lipídicas individuales en células de mamíferos con una precisión y detalle sin precedentes. Este logro no es meramente una mejora incremental; representa un salto cualitativo que está reescribiendo nuestra comprensión del flujo lipídico celular y abriendo nuevas avenidas para explorar las bases moleculares de enfermedades metabólicas y neurodegenerativas.
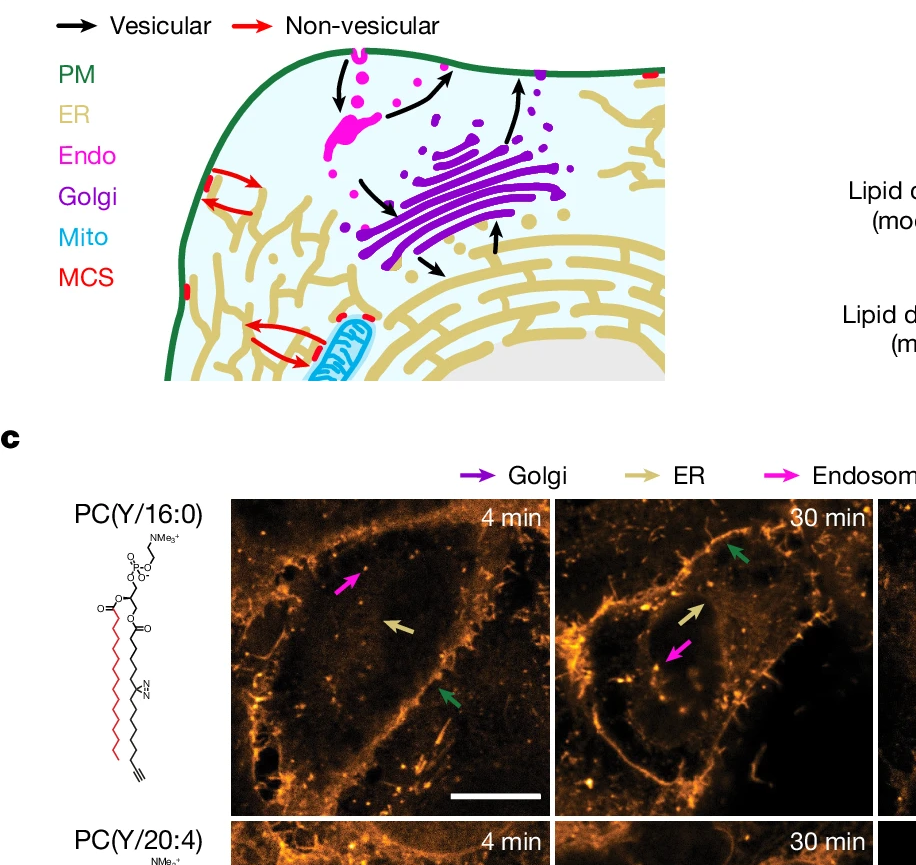
La magia detrás de esta nueva técnica reside en una combinación virtuosa de metodologías de vanguardia. En su núcleo, el método integra la imagen de fluorescencia resuelta en el tiempo de sondas lipídicas bifuncionales, la espectrometría de masas de ultra alta resolución y el modelado matemático. Cada uno de estos componentes, por sí mismo, representa un campo de especialización complejo, pero su sinergia ha permitido a los científicos superar las limitaciones anteriores.
Las “sondas lipídicas bifuncionales” son moléculas ingeniosamente diseñadas que actúan como pequeños detectives moleculares. Estos lípidos artificiales se insertan en las membranas celulares y llevan consigo una etiqueta fluorescente. La parte “bifuncional” implica que estas sondas no solo imitan a los lípidos naturales para ser transportadas, sino que también emiten luz de una manera que cambia con el tiempo y el entorno, permitiendo a los investigadores rastrear su movimiento y su destino en tiempo real. Al observar cómo la fluorescencia de estas sondas decae y se comporta, los científicos pueden deducir la velocidad y la trayectoria de los lípidos a medida que navegan por el laberinto celular.
Para complementar la visión dinámica proporcionada por la fluorescencia, el equipo recurrió a la espectrometría de masas de ultra alta resolución. Esta técnica es como una balanza molecular increíblemente sensible, capaz de identificar y cuantificar con precisión las especies lipídicas presentes en diferentes compartimentos celulares. Al combinar esta “huella dactilar” molecular con los datos de movimiento, los investigadores pudieron obtener una imagen completa de qué lípidos se estaban moviendo y en qué cantidades. Finalmente, el modelado matemático fue la clave para integrar toda esta información, creando un marco predictivo que describe el flujo de lípidos en la célula, permitiendo a los científicos no solo observar, sino también entender las reglas que rigen este intrincado sistema.
Los hallazgos de este estudio son, en una palabra, revolucionarios. La revelación más impactante es que el transporte de lípidos direccional y no vesicular no solo es significativamente más rápido, sino también considerablemente más selectivo que el tráfico vesicular, el cual tradicionalmente se pensaba que era el principal motor. Para poner esto en perspectiva, los investigadores descubrieron que este mecanismo no vesicular es responsable del 85-95% del transporte retrógrado de lípidos desde la membrana plasmática y es hasta 11 veces más rápido que el transporte mediado por vesículas.
¿Qué significa esto para nuestra comprensión fundamental de la célula? Significa que la célula no depende únicamente de camiones de reparto (vesículas) para mover todos sus lípidos. Hay vías “rápidas” o “expresas” que operan de manera mucho más eficiente y con una especificidad asombrosa. Imaginen que, en lugar de esperar a que un camión entregue un paquete a una dirección específica, el paquete pudiera ser teletransportado o transportado por un mensajero ultrarrápido directamente a su destino exacto. Esto sugiere la existencia de una red de transporte de lípidos mucho más sofisticada y dinámica de lo que se creía, donde los lípidos pueden moverse directamente entre orgánulos en puntos de contacto, o a través de proteínas transportadoras en el citoplasma, sin necesidad de ser encapsulados en vesículas.
Pero, ¿cómo logra la célula esta especificidad y rapidez sin el envoltorio de una vesícula? Aquí entra en juego otro actor crucial desvelado por el estudio: las P4-ATPasas. Estas proteínas son bombas lipídicas dependientes de energía que se encargan del “flipping” o volteo de lípidos, moviéndolos de una capa a otra dentro de la bicapa lipídica de la membrana. Esencialmente, estas P4-ATPasas actúan como porteros moleculares, asegurando que los lípidos correctos estén en el lado correcto de la membrana y, al hacerlo, ayudan a mantener las composiciones lipídicas específicas de cada orgánulo. La investigación ha demostrado que este transporte no vesicular está intrínsecamente acoplado con la actividad de “flipping” de las P4-ATPasas. Esto no solo proporciona un mecanismo para el movimiento direccional, sino también para la increíble selectividad observada, garantizando que cada orgánulo mantenga su identidad lipídica única, un requisito indispensable para su función.
El descubrimiento de esta vía de transporte no vesicular, dominante y energéticamente dependiente, representa un cambio de paradigma en la biología celular. Es como si hubiéramos estado observando el tráfico en una ciudad y solo hubiéramos contado los camiones, sin darnos cuenta de que una red de motocicletas y drones ultrarrápidos estaba realizando la mayor parte de las entregas críticas y urgentes. Esta nueva perspectiva ofrece un “mapa integral del flujo lipídico” en las células, proporcionando una comprensión mucho más granular y dinámica de cómo se gestionan y distribuyen los lípidos en un organismo vivo.
Las implicaciones de este descubrimiento son profundas y se extienden a un amplio espectro de enfermedades. Los lípidos no son solo grasa inerte; son componentes vitales en la señalización celular, el metabolismo energético y la estructura de sistemas complejos como el nervioso.
En el ámbito de las enfermedades metabólicas, una comprensión más profunda del transporte lipídico podría ser revolucionaria. Afecciones como la obesidad, la diabetes tipo 2 y las enfermedades hepáticas grasas no alcohólicas se caracterizan por desregulaciones en el metabolismo y almacenamiento de lípidos. Si el transporte no vesicular es el principal mecanismo para mover lípidos clave, entonces las disfunciones en estas vías podrían ser directamente responsables de la acumulación anómala de lípidos o de la distribución incorrecta, lo que lleva a la patología. Por ejemplo, entender cómo los triglicéridos o el colesterol son transportados entre el retículo endoplasmático, las gotitas lipídicas y la membrana plasmática podría revelar nuevos objetivos terapéuticos para controlar estas enfermedades crónicas que afectan a millones de personas en todo el mundo. Las enzimas y proteínas implicadas en este transporte no vesicular, especialmente las P4-ATPasas, podrían convertirse en el foco de nuevas investigaciones farmacéuticas para desarrollar fármacos que modulen el flujo de lípidos y restauren el equilibrio metabólico.
De manera similar, las enfermedades neurodegenerativas como el Alzheimer, el Parkinson y la esclerosis múltiple, a menudo tienen componentes lipídicos subyacentes. El cerebro es el órgano más rico en lípidos del cuerpo, y el mantenimiento de la composición lipídica específica de las neuronas, la mielina (la capa aislante de los axones) y las células gliales es vital para la función cerebral. Alteraciones en el transporte de lípidos pueden llevar a la disfunción sináptica, la degeneración neuronal y la pérdida de la integridad de la mielina. Por ejemplo, en la enfermedad de Alzheimer, se ha demostrado que las placas amiloides y los ovillos neurofibrilares interactúan con los lípidos, y el metabolismo del colesterol es un factor de riesgo conocido. Si el transporte no vesicular es el mecanismo predominante para mover estos lípidos cruciales en las neuronas, entonces la identificación de fallos en estas vías podría ofrecer nuevas perspectivas sobre la progresión de la enfermedad y el desarrollo de terapias. Podría ser que las disfunciones en proteínas como las P4-ATPasas en células neuronales contribuyan directamente a la acumulación de lípidos tóxicos o a la deficiencia de lípidos esenciales, desencadenando la cascada neurodegenerativa.
Además, este conocimiento podría arrojar luz sobre enfermedades raras, conocidas como trastornos del almacenamiento de lípidos, donde la acumulación anormal de lípidos en ciertas células y tejidos conduce a una variedad de síntomas devastadores. Al mapear el flujo lipídico con una precisión sin precedentes, los científicos podrían identificar exactamente dónde se están produciendo los cuellos de botella o las desviaciones en el transporte, lo que permitiría diseñar intervenciones mucho más dirigidas y efectivas.
En última instancia, el valor de esta investigación trasciende la mera curiosidad académica. Al proporcionarnos una visión cuantitativa y sin precedentes del transporte de lípidos, este estudio nos equipa con una herramienta poderosa para desentrañar las complejidades de la biología celular y sus patologías. Los mapas detallados del flujo lipídico que ahora pueden generarse serán invaluables para la comunidad científica. Permitirán a los investigadores no solo identificar los mecanismos fundamentales que gobiernan la vida celular, sino también pinchar y manipular estas vías en modelos de enfermedad para probar nuevas hipótesis y desarrollar estrategias terapéuticas innovadoras. El futuro de la investigación en enfermedades metabólicas y neurodegenerativas parece ahora un poco más brillante, guiado por la luz de este nuevo mapa del intrincado mundo del transporte lipídico celular. Es un testimonio del poder de la innovación tecnológica y la colaboración interdisciplinaria para desvelar los secretos más íntimos de la vida.
Referencia Original:
Iglesias-Artola, J.M., Böhlig, K., Schuhmann, K. et al. Quantitative imaging of lipid transport in mammalian cells. Nature (2025). https://doi.org/10.1038/s41586-025-09432-x