En pocas palabras
Incluso con los modernos tratamientos antirretrovirales (TAR), las personas con VIH (PVVIH) sufren de una inflamación crónica causada por un “intestino permeable”. Un estudio revolucionario ha descubierto al sorprendente culpable: las propias células inmunitarias del paciente. En concreto, las células T CD8+ que residen en el colon, encargadas de protegernos, se vuelven disfuncionales.
Los científicos descubrieron que en estas células se apaga un sensor metabólico clave llamado PPARγ, que es esencial para el metabolismo de las grasas. Al no poder usar sus propias reservas de energía, estas células T “hambrientas” se convierten en una especie de “vampiros celulares”: se adhieren físicamente a las células del revestimiento intestinal y les roban los lípidos de sus membranas para sobrevivir. Este acto de “canibalismo” celular es fatal para las células intestinales, provocando su muerte (apoptosis) y creando la permeabilidad en la barrera intestinal. La buena noticia es que el estudio demostró que tratar estas células T con un fármaco que reactiva el sensor PPARγ “sacia” a las células inmunes, deteniendo el ataque y restaurando su función normal. Este hallazgo abre una nueva y prometedora vía terapéutica para sanar el intestino y reducir la inflamación crónica en las PVVIH.

VIH y la barrera del intestino
Los tratamientos antirretrovirales (TAR) han sido uno de los mayores triunfos de la medicina moderna. Han transformado una sentencia de muerte en una condición crónica manejable, permitiendo a las personas con VIH (PVVIH) vivir vidas largas y plenas. Sin embargo, un fantasma ha persistido, una complicación silenciosa que la medicación no ha podido erradicar por completo: la inflamación crónica. Su origen se encuentra en el intestino, en una condición conocida como “intestino permeable”, donde la barrera que nos protege del contenido intestinal se debilita. Este problema no solo causa malestar, sino que está directamente relacionado con un mayor riesgo de enfermedades cardíacas, diabetes y envejecimiento prematuro en esta población.
El “porqué” de este daño persistente era un profundo misterio. Ahora, un estudio publicado en la prestigiosa revista Cell ha resuelto el enigma, y la respuesta es tan inesperada como fascinante. Los culpables no son agentes externos, sino los propios soldados de élite de nuestro sistema inmunitario, que, debido a un fallo metabólico, se convierten en verdaderos “vampiros celulares”.
La escena del crimen: la barrera intestinal
Imagina la pared de tu intestino como una muralla de ladrillos perfectamente sellada. Su función es absorber nutrientes mientras mantiene a raya a las bacterias y toxinas del interior. En las PVVIH, incluso con el virus bajo control, esta muralla presenta grietas. Los productos microbianos se filtran al torrente sanguíneo, activando constantemente al sistema inmunitario y generando una inflamación sistémica.
Los investigadores, usando biopsias de colon de personas con y sin VIH, confirmaron que el revestimiento intestinal de las PVVIH mostraba una alta tasa de muerte celular (apoptosis). La pregunta era: ¿quién estaba matando a estas células?

El giro inesperado: cuando los guardianes se vuelven agresores
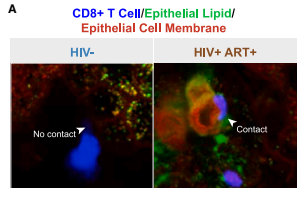
Las sospechas recayeron sobre las células T CD8+, también conocidas como “células T asesinas”. Estos son los soldados de élite de nuestro sistema inmunitario, especializados en patrullar los tejidos y eliminar células infectadas o cancerosas. El equipo descubrió que, en el colon de las PVVIH, estas células T CD8+ se encontraban anormalmente cerca de las células epiteliales moribundas, sugiriendo una interacción directa.
Pero aquí estaba la paradoja: estas células T no estaban funcionando como asesinas convencionales. No estaban liberando sus armas citotóxicas habituales. El ataque era de otra naturaleza, una mucho más sutil y metabólica.

El motivo: el hambre de un soldado
La clave del misterio se reveló al estudiar el metabolismo de estas células T. Los investigadores descubrieron que, en las células T del colon de las PVVIH, un gen crucial llamado PPARγ estaba prácticamente “apagado”. PPARγ es un “sensor maestro” que regula cómo las células utilizan y almacenan las grasas (lípidos). Las células T saludables, como cualquier soldado de élite, necesitan una enorme cantidad de energía, y su principal combustible son los ácidos grasos, que obtienen de sus propias reservas internas, almacenadas en pequeñas gotas de lípidos.

Sin el sensor PPARγ, las células T de las PVVIH eran incapaces de gestionar sus reservas de grasa. Estaban, en esencia, metabólicamente rotas y hambrientas. A pesar de estar rodeadas de nutrientes, no podían acceder a su propio combustible.
Y aquí es donde se produce el acto de desesperación biológica. Para sobrevivir, estas células T hambrientas hacen algo extraordinario: utilizan su maquinaria de contacto para adherirse físicamente a las células epiteliales vecinas y, literalmente, les roban trozos de su membrana rica en lípidos. Se convierten en vampiros celulares, alimentándose de sus vecinas para mantenerse con vida. Este acto de “canibalismo” o “lipid scavenging” es fatal para la célula epitelial, que no puede sobrevivir a la pérdida de su membrana y entra en apoptosis.

La esperanza: un fármaco para “saciar” a los vampiros
El descubrimiento de este mecanismo no solo es fascinante, sino que también ofrece una solución. Si el problema es que el sensor PPARγ está apagado, ¿qué pasaría si lo volviéramos a encender?
Los científicos trataron las células T “vampíricas” con un fármaco ya conocido, un agonista de PPARγ (una molécula que activa el receptor). El resultado fue espectacular. Al reactivar el sensor, las células T recuperaron su capacidad para gestionar sus propias reservas de lípidos. Dejaron de estar hambrientas y, en consecuencia, dejaron de atacar a las células epiteliales. La muerte celular en los cultivos de organoides intestinales se detuvo.
Este estudio es un avance monumental. No solo explica por fin una de las complicaciones más importantes del VIH a largo plazo, sino que identifica un objetivo terapéutico claro y prometedor. Al entender que el problema no es de agresión, sino de metabolismo, se abre la puerta a nuevas terapias que, en lugar de suprimir el sistema inmunitario, lo “reparen” y lo “reeduquen”. Es una nueva y poderosa estrategia para sanar la barrera intestinal, apagar el fuego de la inflamación crónica y mejorar radicalmente la calidad de vida de millones de personas que viven con el VIH.
Referencia del artículo
Das Adhikari, U., Froehle, L. M., Pipkin, A. N., Ringel, A. E., Yilmaz, Ö. H., & Kwon, D. S. (2025). Immunometabolic defects of CD8+ T cells disrupt gut barrier integrity in people with HIV. Cell, 188, 1-14. https://doi.org/10.1016/j.cell.2025.08.024