📌 RESUMEN
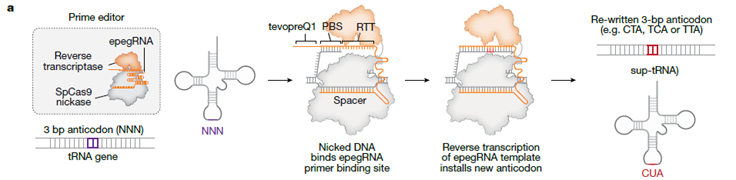
- La Innovación: PERT utiliza Prime Editing para modificar permanentemente un gen de tRNA endógeno redundante en el genoma del paciente, convirtiéndolo en un tRNA supresor (sup-tRNA) optimizado.
- El Mecanismo: Este sup-tRNA reconoce el codón de stop prematuro y, en lugar de detener la traducción, inserta un aminoácido, permitiendo que la proteína se complete.
- Eficacia y Seguridad: Demostraron rescate funcional en modelos celulares de Fibrosis Quística, Tay-Sachs y Batten. En ratones con Síndrome de Hurler, una sola inyección rescató la patología casi por completo.
- Ventaja: A diferencia de terapias anteriores que requerían sobreexpresión masiva de tRNAs (tóxico), PERT funciona a niveles fisiológicos y no afecta la traducción de proteínas normales.

Investigadores del Instituto Broad y Harvard presentan una estrategia universal para corregir mutaciones “sin sentido” (nonsense mutations), convirtiendo ARN de transferencia en supresores de stop prematuros.
La medicina de precisión enfrenta un cuello de botella logístico y económico: existen más de 200,000 mutaciones patogénicas conocidas, y desarrollar un fármaco de edición genética para cada una es inviable. Sin embargo, el 24% de estas enfermedades comparten la misma causa raíz: un codón de stop prematuro (PTC) que trunca la proteína antes de tiempo. Un nuevo estudio publicado en Nature (2025) introduce PERT (Prime Editing-mediated Readthrough of Premature Termination Codons), una tecnología capaz de rescatar la función proteica independientemente del gen afectado.

🧬 Contexto Biológico: El problema de los Codones Stop
Cuando un ribosoma encuentra un codón de stop (UAA, UAG, UGA), la síntesis de proteínas se detiene. En enfermedades genéticas “nonsense”, este stop aparece antes de tiempo, produciendo proteínas truncas e inútiles.
La idea de usar tRNAs supresores (que reconocen el stop y añaden un aminoácido) no es nueva, pero tenía problemas graves:
- Toxicidad: Para que funcionaran, había que inyectar cantidades masivas, lo que alteraba la traducción global de la célula.
- Duración: Los tratamientos eran temporales.

🛠️ La Metodología (The Toolbox)
El equipo de David R. Liu aplicó ingeniería evolutiva y edición de precisión:
- Cribado Masivo: Evaluaron miles de variantes de tRNAs humanos para encontrar aquellos que, incluso a baja concentración, fueran potentes supresores.
- Optimización Estructural: Modificaron no solo el anticodón, sino también el tallo aceptor y las secuencias líder/terminador para maximizar la eficiencia y estabilidad.
- Prime Editing: Usaron esta técnica (que escribe ADN nuevo sin romper la doble hélice) para reescribir un gen de tRNA endógeno en el genoma, convirtiéndolo en la versión “supresora” de forma permanente.
⚙️ Lógica Biológica: ¿Por qué no es tóxico?
La gran pregunta es: ¿Si el sup-tRNA lee codones de stop, no arruinará todas las proteínas normales al impedir que terminen?
El estudio demuestra que NO, debido a mecanismos de seguridad celular:
- Contexto: Los codones de stop naturales (NTC) tienen señales de terminación robustas (múltiples stops en fila, factores de liberación eficientes en el 3′ UTR) que los hacen resistentes a la supresión.
- Degradación: Si ocurre una lectura errónea en un gen normal, la proteína extendida suele ser degradada rápidamente sin causar daño.
- Niveles Fisiológicos: Al editar un gen endógeno, el sup-tRNA se produce a niveles naturales, evitando la saturación del ribosoma.
📉 Impacto Fenotípico y Clínico
En un modelo de ratón para el Síndrome de Hurler (una enfermedad lisosomal devastadora), el tratamiento con PERT restauró la actividad de la enzima IDUA lo suficiente para eliminar la acumulación patológica de glicosaminoglicanos en cerebro e hígado.
Esto prueba que no se necesita corregir el 100% de las proteínas; con restaurar un pequeño porcentaje (6-10%), se puede curar la enfermedad.

🌍 Perspectivas
PERT es un avance monumental hacia la medicina genómica agnóstica de enfermedad. En lugar de crear 1,000 drogas para 1,000 mutaciones, podríamos tener una sola composición terapéutica (el editor del tRNA) que sirva para miles de pacientes con Fibrosis Quística, Distrofia Muscular de Duchenne y muchas otras, siempre que su causa sea un codón stop prematuro.
📖 Referencia Completa:
Pierce, S. E., Erwood, S., Oye, K., et al., & Liu, D. R. (2025). Prime editing-installed suppressor tRNAs for disease-agnostic genome editing. Nature. Published online: 19 November 2025. https://doi.org/10.1038/s41586-025-09732-2