📌 RESUMEN
- La Innovación: Crearon CREST (Cell-engineered Receptive Endometrial Scaffold Technology), un andamio 3D que imita la arquitectura y rigidez del útero humano, poblado con células endometriales reales.
- El Logro: Embriones humanos y “blastoides” (modelos de embrión hechos de células madre) lograron implantarse, invadir el tejido y desarrollar estructuras complejas como el saco vitelino y la placenta primitiva (sincitiotrofoblasto).
- El Descubrimiento: Identificaron una señalización clave (vía PROS1-AXL) entre el embrión y el útero. Si esta comunicación falla, la placenta no crece. Esto podría explicar muchos casos de infertilidad y abortos espontáneos.

Científicos desarrollan CREST, un modelo de endometrio humano in vitro que permite, por primera vez, observar y analizar la implantación del embrión y el inicio de la placenta en tiempo real.
La implantación del embrión humano es una “caja negra”. Ocurre en lo profundo del útero, días después de la fertilización, y es el momento crítico donde fallan la mayoría de los embarazos (naturales y por FIV). Estudiarlo en vivo es éticamente imposible y técnicamente inviable. Pero un equipo internacional liderado por la Universidad de Cambridge y el Instituto Babraham ha roto esa barrera. Publicado en Cell (2026), presentan un modelo de endometrio bioingenieril que no solo acepta embriones humanos, sino que dialoga con ellos, permitiendo el desarrollo de estructuras placentarias avanzadas nunca antes vistas en el laboratorio.
🧬 Contexto Biológico: La “Ventana de Implantación”
El útero no siempre acepta embriones; solo lo hace durante una breve “ventana de implantación” controlada por hormonas. Fuera de ese tiempo, es hostil.
- El problema: Los modelos anteriores (líneas celulares en 2D) no tenían la arquitectura 3D ni la complejidad celular para simular este proceso. Los embriones cultivados en plástico no se organizan correctamente.
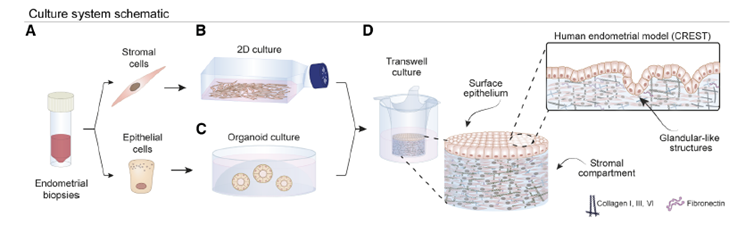
- La solución: CREST recrea el estroma (soporte) y el epitelio (superficie) del útero, y responde a hormonas (estrógeno y progesterona) cambiando su forma y secretando “leche uterina” (glucodelina), tal como lo hace el cuerpo de una mujer.
🛠️ La Metodología (The Toolbox)
El equipo combinó ingeniería de tejidos con biología celular de vanguardia:

- Bioingeniería: Usaron un hidrogel de dextrano entrecruzado con péptidos degradables, enriquecido con colágeno y fibronectina para imitar la matriz extracelular uterina.
- Cultivo Celular: Poblaron este gel con células del estroma y del epitelio obtenidas de biopsias de mujeres fértiles.
- Análisis Ómico: Realizaron scRNA-seq (secuenciación de ARN de célula única) en el sitio de implantación (día 14) para leer los “mensajes” químicos que se envían las células del embrión y las del útero.


⚙️ El Mecanismo Molecular: Diálogo Materno-Fetal
El estudio reveló que la implantación no es una invasión unilateral del embrión, sino una conversación.
- Señalización PROS1-AXL: Descubrieron que el trofoblasto (la futura placenta) secreta una proteína llamada PROS1. Esta viaja a las células del útero, activando el receptor AXL.
- Respuesta del Estroma: Al activarse AXL, las células del útero modifican su comportamiento para permitir y guiar la invasión del embrión.
- Prueba de Concepto: Al bloquear el receptor AXL con un fármaco (R428), el embrión intentó implantarse, pero la placenta no pudo crecer ni expandirse. El “diálogo” se rompió.

📉 Impacto Clínico y Ético
Este modelo tiene implicaciones gigantescas:
- FIV: Permitirá entender por qué fallan tantos tratamientos de fertilidad. Podríamos crear modelos personalizados con células de una paciente para probar si su útero es receptivo antes de transferir un embrión.
- Enfermedades del Embarazo: Ayudará a estudiar el origen de la preeclampsia y la restricción de crecimiento intrauterino desde sus primerísimos momentos.
- Anticoncepción: Podría usarse para probar nuevos anticonceptivos que impidan la implantación sin hormonas sistémicas.
📖 Referencia Completa:
Molè, M. A., Elderkin, S., Zorzan, I., et al. (2026). Modeling human embryo implantation in vitro. Cell, 189, 1–19. https://doi.org/10.1016/j.cell.2025.10.027