📝 RESUMEN
Más del 20% de las enfermedades genéticas hereditarias son causadas por “mutaciones de cambio de pauta de lectura” (frameshift), un error catastrófico que arruina la producción de proteínas vitales. Reparar esto dentro del cuerpo era casi imposible porque las células no aceptan fácilmente “plantillas” de ADN de repuesto. Sin embargo, un nuevo estudio publicado en Nature Biomedical Engineering presenta TIGER, una plataforma basada en CRISPR que predice y manipula los mecanismos naturales de reparación celular para restaurar el gen dañado sin necesidad de plantillas. Con una eficacia sin precedentes, este sistema logró curar modelos animales de ceguera genética (retinitis pigmentosa) y obesidad severa (síndrome de Alström), abriendo una nueva era para la medicina de precisión.

1. Introducción: El Problema de “Leer” el ADN 📖🔍
Para entender la magnitud de este avance, primero debemos entender cómo lee la célula nuestro ADN. Imagina que el genoma es un libro donde todas las palabras tienen exactamente tres letras. Si la frase dice: “LOS DOS VAN SIN LUZ”, la célula la lee correctamente.
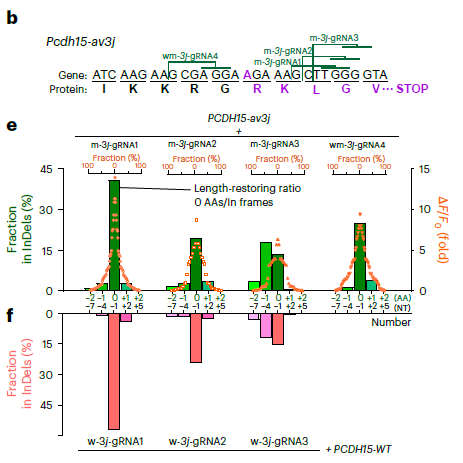
Pero, ¿qué pasa si una mutación elimina o añade una sola letra al principio? Si quitamos la ‘L’ de ‘LOS’, la pauta de lectura se recorre, y la frase se convierte en: “OSD OSV ANS INL UZ”. Esto es una mutación de cambio de marco de lectura (frameshift). A partir del error, toda la proteína generada será un completo desastre o se destruirá.
Las herramientas tradicionales de CRISPR intentaban arreglar esto mediante la recorte del ADN y la inserción de una “plantilla” correcta para que la célula la copiara (un proceso llamado HDR). El gran problema es que las células de nuestro cuerpo (especialmente las neuronas o las del ojo) casi nunca usan este método de copia, prefiriendo simplemente reparar los extremos rotos a la fuerza (NHEJ), lo que suele generar más errores. Estábamos estancados… hasta ahora.

2. TIGER: Hackeando la Reparación Celular 🐅✂️
Los investigadores crearon la plataforma TIGER (Template-Independent Genome Editing for Restoration). En lugar de luchar contra la tendencia de la célula a pegar los extremos a la fuerza, decidieron predecirla y usarla a su favor.
Descubrieron que la forma en que la célula repara el corte de Cas9 no es totalmente aleatoria; depende de la secuencia exacta de letras alrededor del corte. TIGER utiliza un sofisticado sistema de puntuación para diseñar un ARN guía (gRNA) perfecto que obliga a la célula a cometer un error de reparación matemáticamente calculado que, por pura coincidencia dirigida, vuelve a alinear la frase original.

3. Puntos Clave del Descubrimiento 🎯📊
- Eficacia arrolladora: El sistema logró generar productos con el marco de lectura restaurado en aproximadamente el 75% de las mutaciones por deleción (pérdida de letras) y en el 50% de las mutaciones por inserción (ganancia de letras). Esto es más que suficiente para que el cuerpo recupere su función normal.
- Versatilidad universal: TIGER funciona con diferentes variantes de la enzima Cas9 (como SpCas9, SaCas9 y AsCas12a), lo que permite a los científicos adaptar el tratamiento a distintos tamaños de virus transportadores para llegar a casi cualquier órgano del cuerpo.
- Diseño eficiente: Los investigadores analizaron más de 3.2 millones de eventos de reparación genética en distintos tipos de células y tejidos para alimentar su algoritmo predictivo, asegurando que el tratamiento sea preciso independientemente del órgano objetivo.

4. Del Laboratorio a la Vida Real: Ratones Curados 🐁✨
Para demostrar que esto no es solo teoría, el equipo probó TIGER en modelos vivos de ratón con resultados espectaculares:
- Retinitis Pigmentosa: En ratones que iban a quedar ciegos por una mutación en el gen Pde6b, TIGER logró editar directamente las células de la retina in vivo, restaurando la función de los fotorreceptores y rescatando su visión.

- Síndrome de Alström: Trataron crías de ratón con una mutación en el gen Alms1, que causa hiperfagia (hambre extrema) y obesidad mórbida. La terapia en el hipotálamo del cerebro restauró la proteína perdida, lo que redujo significativamente el peso corporal y revirtió la disfunción metabólica.

📚 REFERENCIA BIBLIOGRÁFICA
Qiu, S., Liu, L., Xiang, B., Jin, Z., Li, Y., Li, D., Hou, H., Li, K., Wei, G., Xie, J., Li, S., Liu, S., Chen, C., Liang, X., Sun, Q., & Xiong, W. (2026). Template-independent genome editing and restoration for correcting frameshift disorders. Nature Biomedical Engineering. https://doi.org/10.1038/s41551-026-01635-5