En el mundo de la biología de mamíferos, la determinación del sexo se ha entendido clásicamente como una batalla entre dos programas genéticos opuestos: uno que favorece el desarrollo masculino y otro el femenino. Las reglas biológicas dictan que la presencia de un cromosoma Y (y su gen clave Sry) activa un gen maestro llamado Sox9, el cual da la orden de construir testículos. Por el contrario, en los individuos genéticamente hembras (XX), este gen Sox9 debe mantenerse estrictamente apagado para permitir que el ovario se desarrolle en paz. Sin embargo, ¿qué pasaría si te dijéramos que una simple “falta de ortografía” de una sola letra en todo nuestro inmenso código genético es suficiente para anular por completo las reglas de los cromosomas sexuales? Un nuevo y fascinante artículo científico acaba de revelar que alteraciones microscópicas en el ADN pueden provocar que un organismo XX se desarrolle completamente como un macho.
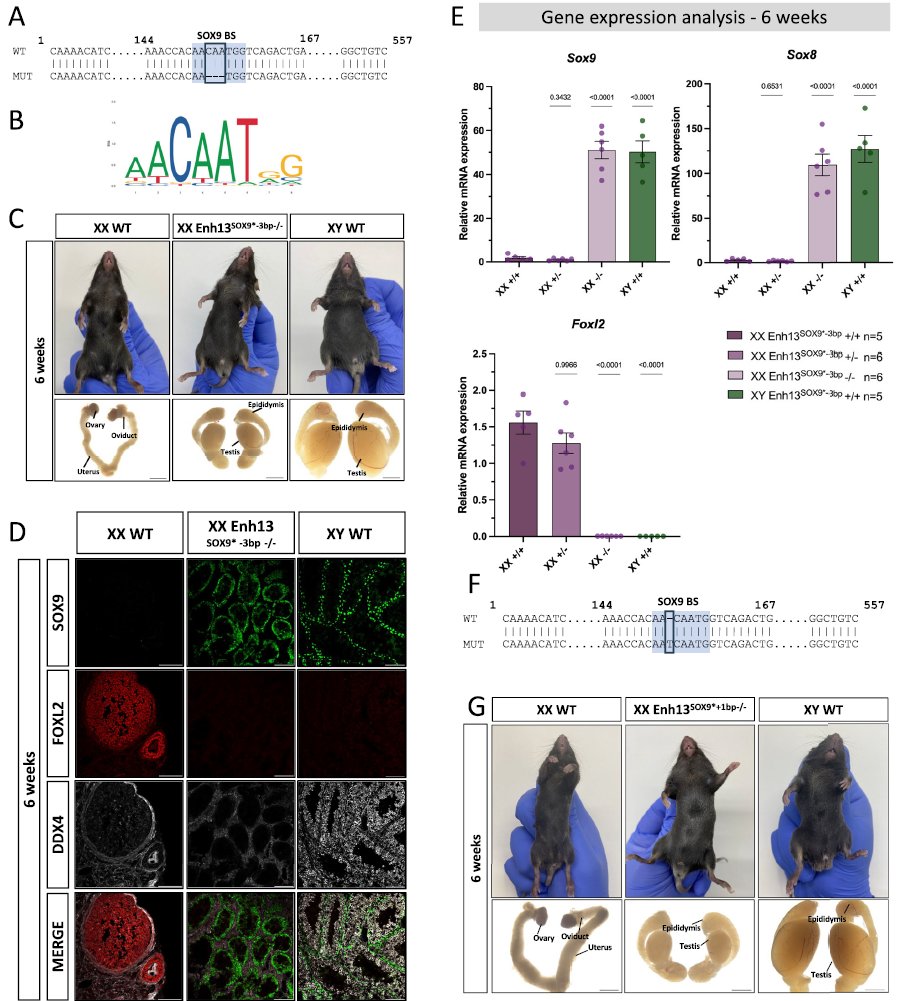
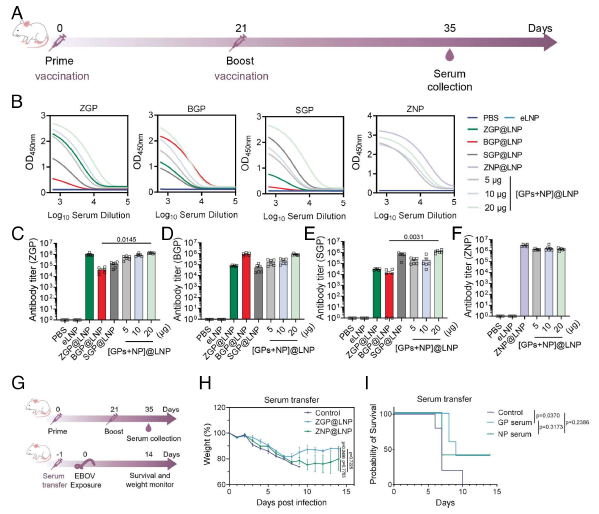
Para desentrañar este misterio, los investigadores centraron su atención en el “Enhancer 13” (o Enh13), un interruptor regulador ubicado a gran distancia del gen Sox9. Sabían que este interruptor era vital para el desarrollo testicular, pero querían entender su nivel de sensibilidad. Utilizando la herramienta de edición genética CRISPR, introdujeron cambios extremadamente sutiles en el Enh13 de embriones de ratón genéticamente hembras (XX): en algunos eliminaron apenas 3 pares de bases (letras de ADN) y en otros insertaron tan solo 1 base. Contra todo pronóstico, estos diminutos cambios en el interruptor fueron suficientes para causar una reversión sexual completa de hembra a macho. Al llegar a la edad adulta, los ratones XX mutados lucían externa e internamente como machos, desarrollando testículos en lugar de ovarios, aunque carecían de espermatozoides funcionales debido a la ausencia natural de los genes del cromosoma Y. A continuación, podemos ver cómo lucen estos ratones:

Caracterización de los ratones adultos con la deleción de 3 letras o la inserción de 1 letra. Las imágenes muestran cómo, a pesar de ser genéticamente XX (hembras), ambos grupos de ratones mutantes desarrollan genitales externos masculinos y testículos internos (aunque más pequeños que los de los machos XY silvestres debido a la falta del cromosoma Y).
¡GRACIAS POR LEER NUESTRAS NOTICIAS! ¿Nos invitas un cáfe? ☕
Pero, ¿cómo es posible que un cambio tan minúsculo pueda tener un impacto fisiológico tan masivo? Al investigar el desarrollo embrionario de estos animales, el equipo descubrió que la clave no estaba en que la mutación “encendiera” mágicamente el interruptor, sino en que arruinaba el “freno” biológico. En un embrión XX normal, el Enh13 funciona como un punto de anclaje donde varias proteínas pro-femeninas (como el factor RUNX1) se unen fuertemente para reprimir y silenciar al gen Sox9. Los investigadores descubrieron que eliminar 3 letras o agregar 1 letra no destruye el sitio donde se unen estas proteínas, sino que altera la distancia física entre ellas.
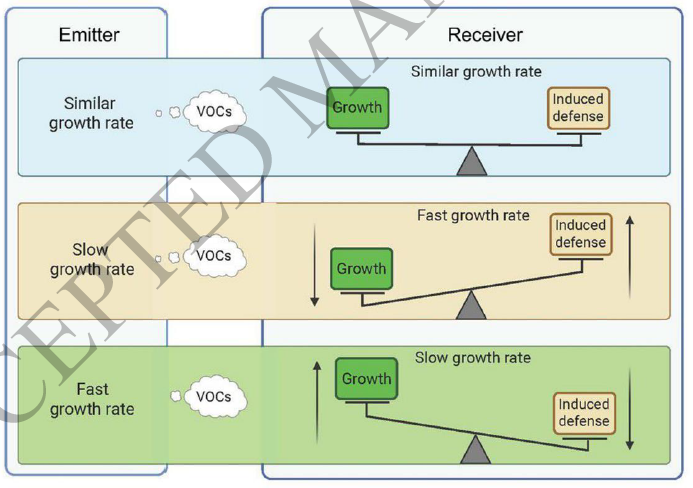
El genoma es una estructura tridimensional, y en este caso, la mutación acerca físicamente al represor RUNX1 con otra proteína llamada GATA4 en la cadena de ADN. En el caso de la inserción de una sola letra, la mutación es tan precisa que crea un sitio de unión completamente nuevo para GATA4 justo al lado de RUNX1. Esta cercanía antinatural altera la forma en la que estas proteínas cooperan, provocando que pierdan su capacidad represiva. Al fallar este freno, el gen Sox9 logra expresarse un poco, alcanzando un umbral crítico que desencadena una reacción en cadena donde el gen se auto-activa masivamente, ordenando la formación de testículos. El proceso detallado se esquematiza a continuación:

Modelo propuesto del mecanismo del Enh13. En la parte superior (XY y XX WT) se observa cómo el genoma silvestre activa o reprime el gen Sox9 según el sexo. En la parte inferior, se ilustra cómo la mutación de -3bp o +1bp altera físicamente el espacio en el ADN, acercando indebidamente a las proteínas RUNX1 y GATA4. Esto rompe la represión y dispara el desarrollo testicular en individuos XX.
Lo más fascinante de este descubrimiento es la lección que nos deja sobre la “gramática” de la vida. Hasta ahora, a menudo pensábamos en el ADN como una simple secuencia de instrucciones donde perder una letra podría romper una proteína. Sin embargo, este estudio demuestra que el espaciado físico exacto entre los puntos de control del ADN es igual de crítico. Una sola letra adicional puede alterar el abrazo tridimensional de las proteínas reguladoras y reescribir por completo el destino embrionario de un mamífero, abriendo nuevas puertas para comprender los diferentes trastornos del desarrollo sexual en humanos.
——————————————————————————–
Referencia: Abberbock, E., Ridnik, M., Stévant, I., Weiss, R., Bamberger, C., Lhermann, S. Z., … & Gonen, N. (2026). A single-nucleotide enhancer mutation overrides chromosomal sex to drive XX male development. Nature Communications. https://doi.org/10.1038/s41467-026-71328-9.