¡Tu carrito está actualmente vacío!
El Secreto del Agarre de Acero de una Bacteria Común: Cómo el Calcio la Convierte en una Súper-Colonizadora de la Piel
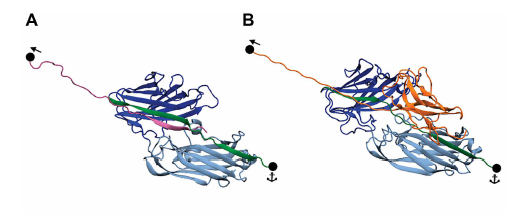
Nuestra piel es un campo de batalla microscópico. Entre los muchos habitantes, la bacteria Staphylococcus aureus es una de las más conocidas. Aunque a menudo vive en paz sobre nosotros, puede convertirse en un invasor oportunista, causando infecciones y, notablemente, empeorando condiciones como la dermatitis atópica (eccema). Un equipo de científicos ha desvelado el asombroso truco molecular que esta bacteria utiliza para aferrarse a nuestra piel con una fuerza casi inquebrantable, revelando un mecanismo de adhesión más fuerte y sofisticado de lo que nadie imaginaba.
1. El Arma de la Bacteria: Un Anclaje con Fuerza de Superhéroe
Los investigadores se centraron en una proteína de la superficie de S. aureus llamada SdrD. Para medir su poder, utilizaron una técnica de vanguardia llamada espectroscopía de fuerza de molécula única. Es como tener unas pinzas nanoscópicas capaces de tomar una sola bacteria y medir la fuerza exacta que se necesita para despegarla de una célula de la piel. Los resultados fueron asombrosos: la unión entre la proteína SdrD de la bacteria y su objetivo en la piel, la desmogleína-1 (DSG-1), soportaba fuerzas superiores a 2 nanonewtons.

Lo más importante: La unión SdrD-DSG-1 es una de las interacciones moleculares no covalentes más fuertes jamás registradas en la biología, lo que explica por qué S. aureus puede colonizar nuestra piel de manera tan persistente y eficaz.

2. Un Agarre Inteligente: Más Fuerte Bajo Presión y con Amortiguador Integrado
El agarre de S. aureus no es solo fuerte, también es inteligente. La interacción funciona como un “enlace de captura” (catch bond), un fenómeno contraintuitivo donde el enlace se vuelve más resistente cuanto más se tira de él. Es el sistema perfecto para sobrevivir en un entorno dinámico como la piel, sujeto a roces y estiramientos.
Además, la propia proteína SdrD está diseñada como una obra maestra de la ingeniería. Posee una serie de dominios repetidos que actúan como un amortiguador molecular. Cuando se aplica una fuerza externa, estos dominios se despliegan uno por uno, disipando la energía y protegiendo el punto de anclaje principal para que no se rompa.

Lo más importante: La bacteria no solo se agarra con fuerza, sino que su anclaje se refuerza bajo estrés mecánico y cuenta con un sistema de amortiguación que le confiere una resiliencia extraordinaria.

3. El Cómplice Inesperado: El Papel Fundamental del Calcio
Aquí es donde reside el descubrimiento más revolucionario del estudio. Los científicos descubrieron que el calcio es el regulador clave de toda esta interacción. Su función es doble y crucial:
- Fortalece a la bacteria: El calcio estabiliza los dominios “amortiguadores” de la proteína SdrD, asegurando que el arma de la bacteria esté correctamente plegada y sea mecánicamente robusta.
- Refuerza nuestra piel (para su propio beneficio): El calcio también se une a la proteína DSG-1 de nuestra piel. Esta unión rigidiza la estructura de la DSG-1 justo en el lugar donde la bacteria se ancla, creando una plataforma de aterrizaje mucho más estable y sólida.

Lo más importante: El calcio actúa como un catalizador de doble acción, fortaleciendo tanto el “gancho” de la bacteria como el “punto de anclaje” en nuestra piel, elevando la fuerza de la unión a niveles sin precedentes.
4. La Conexión con el Eccema: Cuando la Piel Débil se Vuelve un Ancla Perfecta
Este mecanismo tiene implicaciones directas para las personas con dermatitis atópica. En una piel sana, la proteína DSG-1 se localiza en los bordes de las células. Sin embargo, en la piel con eccema, la barrera cutánea está dañada y la DSG-1 se distribuye de forma anormal por toda la superficie celular. Además, los gradientes de calcio de la piel están alterados.
El estudio demostró que en las células de la piel de pacientes con eccema, S. aureus no solo se adhería con más frecuencia y por toda la superficie, sino que la fuerza de adhesión era aún mayor.

Lo más importante: Las condiciones de la piel con dermatitis atópica (distribución anormal de DSG-1 y alteración del calcio) crean un “entorno ideal” que la bacteria explota para amplificar su súper adhesión, lo que probablemente contribuye a empeorar la enfermedad.
5. Implicaciones y Futuro: Hacia Terapias Más Allá de los Antibióticos
Comprender este mecanismo a un nivel tan detallado abre la puerta a nuevas estrategias terapéuticas. En lugar de depender únicamente de los antibióticos, que pueden generar resistencia, se podrían desarrollar tratamientos dirigidos a debilitar este súper agarre. Las posibilidades incluyen:
- Fármacos que bloqueen la interacción entre SdrD y DSG-1.
- Terapias que modulen la concentración de calcio en las capas superficiales de la piel para desestabilizar la unión.
- Anticuerpos monoclonales diseñados para “tapar” el sitio de unión en la DSG-1, impidiendo que la bacteria se ancle.
Lo más importante: Este descubrimiento proporciona un mapa molecular preciso para diseñar terapias innovadoras que, en lugar de matar a la bacteria, simplemente le impidan adherirse, previniendo así la colonización y la infección.
Referencia:
Chantraine, C., Gomes, P. S. F. C., Mathelié-Guinlet, M., Gomes, D. E. B., Zheng, Z., Clowry, J., Turley, M. B., Irvine, A. D., Geoghegan, J. A., Bernardi, R. C., & Dufrêne, Y. F. (2025). Ultrastrong Staphylococcus aureus adhesion to human skin: Calcium as a key regulator of noncovalent interactions. Science Advances, 11(36), eadu7457. DOI: 10.1126/sciadv.adu7457
AI bacterias Biología Sintética CRISPR cáncer envejecimiento Escherichia coli evolución Microbioma microbiota regulación resistencia salud VIH virus
Ultimos Productos
-
Curso de Organismos Modelo en Biología Molecular Febrero 2025
El precio original era: $75.00.$57.00El precio actual es: $57.00. -
Masterclass: Dinámica y Composición de los Condensados Biomoleculares
El precio original era: $80.00.$60.00El precio actual es: $60.00.
Buscar
Últimos Posts
Últimos Comentarios
Categorías
Archivos
- marzo 2026 (5)
- febrero 2026 (15)
- enero 2026 (21)
- diciembre 2025 (20)
- noviembre 2025 (16)
- octubre 2025 (21)
- septiembre 2025 (17)
- agosto 2025 (17)
- julio 2025 (19)
- junio 2025 (24)
- mayo 2025 (26)
- abril 2025 (49)
- marzo 2025 (20)
- febrero 2025 (10)
- enero 2025 (7)
- diciembre 2024 (8)
- noviembre 2024 (23)
- octubre 2024 (7)
Palabras clave
Sígue las noticias
Te invitamos a registrar tus datos como tu correo electrónico para que puedas recibir las últimas noticias y anuncios de Biología Molecular México

By signing up, you agree to the our terms and our Privacy Policy agreement.