¡Tu carrito está actualmente vacío!
Fatiga Cromatínica: La Cicatriz Oculta que Nuestro ADN Nunca Olvida
Resumen
Nuestro ADN sufre daños constantemente, pero las células tienen sistemas notables para repararlos. Durante décadas, asumimos que, una vez que se repara una ruptura de ADN, el problema está resuelto. Sin embargo, un estudio revolucionario publicado en Science ha descubierto que esto no es del todo cierto. Un equipo de investigadores liderado por Susanne Bantele y Jiri Lukas ha revelado que, aunque la secuencia de ADN se repare a la perfección, la herida deja una “cicatriz” invisible y duradera en la arquitectura tridimensional del genoma. Esta cicatriz, que han bautizado como “fatiga cromatínica”, es una alteración del plegamiento del ADN que perjudica la función de los genes cercanos y, de forma crucial, se hereda de una célula a sus hijas. Este descubrimiento revela una nueva forma de memoria biológica del daño, con profundas implicaciones para comprender el envejecimiento, el cáncer y la seguridad de las tecnologías de edición genética, como CRISPR.

El Origami del Genoma: Más Allá de la Secuencia
Para entender la magnitud de este descubrimiento, primero debemos pensar en el genoma no como una simple hebra de letras (A, T, C, G), sino como un complejo y exquisito origami. Dentro del diminuto núcleo de cada una de nuestras células, casi dos metros de ADN deben empaquetarse de forma organizada. Este empaquetamiento, llamado cromatina, no es aleatorio. El ADN se pliega en bucles y dominios tridimensionales precisos, esenciales para su función. Estos pliegues permiten que regiones distantes del genoma, como un “interruptor” (enhancer) y un “motor” (promotor), entren en contacto para activar o inactivar un gen en el momento adecuado. La arquitectura 3D correcta del genoma es, por tanto, tan importante como la secuencia misma.

La Herida Más Grave y el Equipo de Emergencia
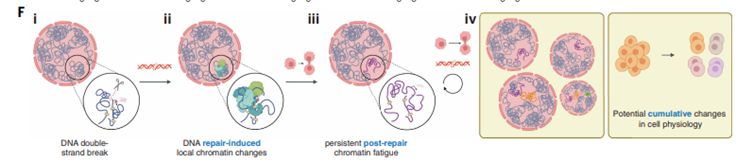
De todos los daños que puede sufrir el ADN, el más catastrófico es la ruptura de doble hebra (DSB), en la que la molécula se divide por completo. Es el “código rojo” de la célula. Para repararlo, la célula despliega un operativo de emergencia masivo. Una de las primeras acciones es “deshacer el origami” localmente: la cromatina se relaja y se reorganiza drásticamente para dar acceso a las maquinarias de reparación.
La gran pregunta que planteó este equipo de investigación fue: ¿qué pasa después? Una vez que las proteínas “reparadoras” han reparado los extremos rotos y la secuencia de ADN vuelve a estar intacta, ¿se vuelve a plegar el origami exactamente como estaba antes? La suposición general era que sí. Este estudio demuestra que no.

Una Herida Quirúrgica para Observar la Cicatriz
Para estudiar este proceso con una precisión sin precedentes, los científicos utilizaron la herramienta de edición genética CRISPR-Cas9 no como un editor, sino como un “bisturí molecular” ultrapreciso. En lugar de causar un daño masivo y caótico con radiación, infligieron una única y solitaria ruptura de doble hebra en un lugar exacto y predeterminado del genoma. El lugar elegido fue el vecindario del gen c-MYC, un importante regulador del crecimiento celular cuyo funcionamiento depende críticamente de la arquitectura 3D que lo rodea.
Mediante técnicas avanzadas de imagen molecular (como DNA FISH) y de mapeo de la estructura 3D del genoma (Micro-C), observaron lo que sucedía antes, durante y, lo más importante, después de la reparación.

El Descubrimiento: Una Memoria Persistente del Daño
Los resultados fueron reveladores. Descubrieron que, incluso días después de que la ruptura del ADN había sido perfectamente reparada y las proteínas reparadoras se habían retirado, la estructura tridimensional de la cromatina nunca volvía a su estado original. El “origami” permanecía mal plegado, “arrugado”. Los bucles y contactos de largo alcance que definían la función del vecindario genético se debilitaban.
A este estado de alteración estructural y funcional persistente lo denominaron fatiga cromatínica. No es una mutación en el código, sino una cicatriz en la forma.

Lo más impactante fue que esta “fatiga” tiene dos consecuencias fundamentales:
- Función Alterada: La fatiga cromatínica actúa como una “sordera” molecular. Los genes dentro de la región afectada, como c-MYC, pierden su capacidad de responder adecuadamente a las señales externas. Por ejemplo, cuando los investigadores estimularon las células con factores de crecimiento, los genes en regiones “fatigadas” se activaron mucho menos que sus contrapartes sanas. La cicatriz había dañado su capacidad de “escuchar”.

- Herencia Epigenética: De forma asombrosa, cuando la célula se dividía, esta cicatriz estructural se transmitía a las células hijas. Las nuevas células, que nunca habían experimentado el daño original, nacían con un genoma ya “fatigado” y funcionalmente deficiente. El daño, por tanto, dejaba una memoria que se heredaba a través de las generaciones celulares.
Las Profundas Implicaciones de la Fatiga Cromatínica
Este descubrimiento cambia fundamentalmente nuestra comprensión del daño en el ADN y tiene implicaciones de gran alcance:
- Envejecimiento: Podría ser uno de los mecanismos que explican por qué envejecemos. A lo largo de la vida, nuestras células acumulan miles de estas “cicatrices”. La suma de estas pequeñas deficiencias funcionales en todo el genoma podría llevar a la pérdida gradual de la función de los tejidos.
- Cáncer: Un gen crucial para el control del cáncer podría quedar en un estado “fatigado”, volviéndolo menos eficiente para responder a señales de estrés y, por tanto, haciendo a la célula más vulnerable a una transformación maligna en el futuro.
- Edición Genética (CRISPR): Esta es quizás la implicación más inmediata y provocadora. Sugiere que incluso una edición genética “perfecta” con CRISPR, que corta y repara el ADN, podría dejar una cicatriz de fatiga cromatínica, afectando de forma no intencionada y permanente la función de los genes vecinos. Es una llamada de atención crucial para la seguridad a largo plazo de las terapias génicas.

Este elegante trabajo nos demuestra que las heridas en nuestro genoma son más profundas de lo que pensábamos. Aunque la célula repare la secuencia, el recuerdo del trauma persiste en su forma, una memoria silenciosa que se transmite a través del tiempo, afectando sutilmente la función celular de maneras que apenas comenzamos a comprender.
Referencia:
Bantele, S., Mordini, I., Biran, A., Alcaraz, N., Zonderland, G., Wenger, A., Krietenstein, N., Groth, A., & Lukas, J. (2025). Repair of DNA double-strand breaks leaves heritable impairment to genome function. Science, 390(6718), 589. https://doi.org/10.1126/science.adk6662
AI bacterias Biología Sintética CRISPR cáncer envejecimiento Escherichia coli evolución Microbioma microbiota regulación resistencia salud VIH virus
Ultimos Productos
-
Curso de Organismos Modelo en Biología Molecular Febrero 2025
El precio original era: $75.00.$57.00El precio actual es: $57.00. -
Masterclass: Dinámica y Composición de los Condensados Biomoleculares
El precio original era: $80.00.$60.00El precio actual es: $60.00.
Buscar
Últimos Posts
Últimos Comentarios
Categorías
Archivos
- marzo 2026 (5)
- febrero 2026 (15)
- enero 2026 (21)
- diciembre 2025 (20)
- noviembre 2025 (16)
- octubre 2025 (21)
- septiembre 2025 (17)
- agosto 2025 (17)
- julio 2025 (19)
- junio 2025 (24)
- mayo 2025 (26)
- abril 2025 (49)
- marzo 2025 (20)
- febrero 2025 (10)
- enero 2025 (7)
- diciembre 2024 (8)
- noviembre 2024 (23)
- octubre 2024 (7)
Palabras clave
Sígue las noticias
Te invitamos a registrar tus datos como tu correo electrónico para que puedas recibir las últimas noticias y anuncios de Biología Molecular México

By signing up, you agree to the our terms and our Privacy Policy agreement.