¡Tu carrito está actualmente vacío!
Hackeando a los Hackers: La Herramienta que Silencia Genes de Virus para Combatir Superbacterias
En pocas palabras
Los bacteriófagos (o fagos) son virus que infectan y matan bacterias, y representan una de nuestras mayores esperanzas en la lucha contra las superbacterias resistentes a los antibióticos. Sin embargo, su inmensa diversidad genética es un “territorio oscuro” del que sabemos muy poco. Estudiar qué hace cada uno de sus genes es extremadamente difícil porque la mayoría de los fagos y bacterias no se pueden modificar genéticamente con las herramientas actuales.
Un nuevo estudio publicado en Nature presenta una solución revolucionaria: una plataforma no genética para silenciar genes de fagos a voluntad. La técnica utiliza pequeñas moléculas sintéticas llamadas oligómeros antisentido (ASOs), que se diseñan a medida para bloquear la producción de una proteína viral específica. Estas moléculas se adhieren a una “llave” molecular que les permite entrar en la bacteria y, una vez dentro, se pegan a las instrucciones genéticas del fago, impidiendo que la maquinaria de la bacteria construya las proteínas virales.
Al aplicar esta técnica a un “fago gigante” que infecta a la bacteria Pseudomonas aeruginosa, los investigadores lograron, por primera vez, apagar sistemáticamente sus genes uno por uno para ver cuáles eran esenciales para la infección. Así, crearon un “mapa de vulnerabilidades” del fago, descubriendo nuevas proteínas cruciales para su ciclo de vida. Esta herramienta universal abre la puerta para estudiar rápidamente cualquier fago en cualquier bacteria, acelerando el descubrimiento de nueva biología y el diseño de terapias con fagos más seguras y eficaces.
¿Y qué hace cada componente de un fago?
En el mundo microscópico se libra una guerra perpetua que ha durado miles de millones de años: la batalla entre las bacterias y los virus que las infectan, los bacteriófagos. Estos fagos son los “hackers” más prolíficos de la naturaleza, máquinas moleculares expertas en infiltrarse y secuestrar la maquinaria celular de una bacteria para su propio beneficio. Paradójicamente, estos antiguos enemigos de las bacterias podrían convertirse en nuestros mayores aliados en la era de la resistencia a los antibióticos. Pero para desplegar este ejército viral de manera segura y eficaz, primero necesitamos entender su manual de instrucciones, y hasta ahora, la mayor parte de ese manual ha estado escrita en un idioma indescifrable.

El gran muro de la genética de fagos
Los fagos son la entidad biológica más abundante en la Tierra, un universo de diversidad genética que apenas hemos comenzado a explorar. La mayoría de sus genes tienen funciones desconocidas. La forma clásica de averiguar qué hace un gen es eliminarlo (hacer un “knockout”) y ver qué le pasa al organismo. El problema es que este enfoque es extremadamente difícil, si no imposible, para la gran mayoría de los pares fago-bacteria. Muchas bacterias, especialmente las “superbacterias” aisladas de pacientes, tienen sistemas de defensa que destruyen cualquier ADN extraño que los científicos intenten introducir, haciendo que la manipulación genética sea una pesadilla. Estábamos ante una biblioteca infinita de conocimiento biológico, pero no teníamos la llave para leer los libros.
El “Control Remoto” Molecular: Oligómeros Antisentido
Un equipo de científicos ha desarrollado una solución elegante y universal para derribar este muro, presentada en un estudio en la revista Nature. Su herramienta no es genética, sino química. Se basa en los oligómeros antisentido (ASOs), que son pequeñas hebras de material sintético diseñadas para ser la imagen especular de una secuencia de ARN mensajero (ARNm) de un gen específico.

Imagina que el gen del fago es un plano y el ARNm es una fotocopia que la bacteria usa para construir una proteína. El ASO es como una tira adhesiva diseñada a medida que se pega justo al principio de la fotocopia. Cuando la maquinaria de la bacteria (el ribosoma) intenta leerla, se encuentra con el ASO bloqueando el camino y no puede construir la proteína. El gen ha sido “silenciado” a nivel de traducción, sin tocar el ADN original.

Para que estos ASOs funcionen, necesitan dos cosas: entrar en la bacteria y ser resistentes a la degradación. Los investigadores lo lograron uniéndolo a un “péptido penetrante de células” (CPP), una especie de llave maestra molecular que les permite atravesar la muralla bacteriana, y construyendo los ASOs con un esqueleto químico sintético (PNA) que los hace invisibles a las enzimas que degradan el material genético.
El mapa de vulnerabilidades de un fago gigante
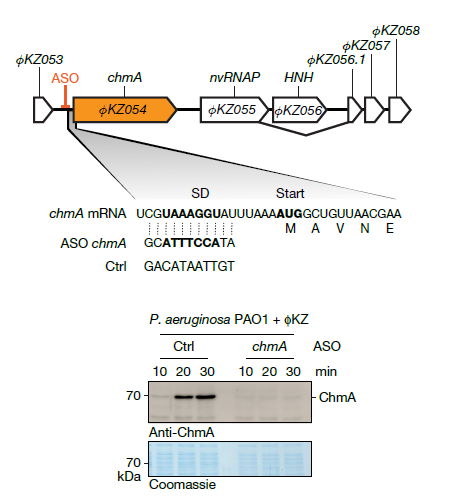
Para demostrar el poder de su herramienta, el equipo la aplicó a un sistema particularmente desafiante: el “fago gigante” ΦKZ, que infecta a la peligrosa bacteria Pseudomonas aeruginosa. Este fago es famoso por construir una estructura similar a un núcleo dentro de la bacteria para proteger su ADN.
Los científicos diseñaron ASOs para 75 genes clave del fago y los probaron uno por uno. Los resultados fueron espectaculares. Al silenciar genes ya conocidos como esenciales, como el que construye la “cáscara” del núcleo viral (el gen chmA), la infección se detenía por completo y la bacteria sobrevivía. Pero lo más emocionante fue el descubrimiento de nuevas vulnerabilidades. Identificaron una proteína hasta ahora enigmática, OKZ155, como un factor crucial. Al silenciar su gen, el núcleo del fago se formaba, pero nunca “maduraba”; era incapaz de replicar su genoma, deteniendo la infección en un punto clave.

Una herramienta universal para una nueva era de la virología
Este estudio es mucho más que el mapeo de un solo fago. Es la demostración de una plataforma universal. Los investigadores demostraron que la técnica funciona en diversas cepas clínicas de Pseudomonas (las que son realmente difíciles de manipular), en otras especies de bacterias e incluso contra diferentes tipos de fagos, incluyendo los que tienen genomas de ARN.
Las implicaciones son enormes:
- Descubrimiento acelerado: Los científicos ahora pueden tomar cualquier fago nuevo y, en cuestión de semanas, tener un mapa de sus genes esenciales, desvelando rápidamente nueva biología.
- Mejora de la terapia con fagos: Permite identificar rápidamente qué genes virales son absolutamente necesarios para matar a la bacteria, ayudando a seleccionar los mejores fagos para un cóctel terapéutico. También permite identificar y silenciar genes que podrían ser problemáticos.
- Elucidar las defensas bacterianas: La técnica también se puede usar a la inversa, silenciando genes de defensa de la bacteria para entender cómo se protege de los virus y cómo los fagos superan esas defensas.
En la lucha contra las superbacterias, necesitamos nuevas armas y, sobre todo, nuevo conocimiento. Esta elegante herramienta de “silenciamiento genético” programable nos proporciona una linterna para explorar la vasta oscuridad del universo viral, prometiendo acelerar el desarrollo de una de las alternativas más prometedoras a los antibióticos: la terapia con fagos.

Referencia del artículo
Gerovac, M., Buhlmann, L., Zhu, Y., Đurica-Mitić, S., Rech, V., Carien, S., … & Vogel, J. (2025). Programmable antisense oligomers for phage functional genomics. Nature. https://doi.org/10.1038/s41586-025-09499-6
AI bacterias Biología Sintética CRISPR cáncer envejecimiento Escherichia coli evolución Microbioma microbiota regulación resistencia salud VIH virus
Ultimos Productos
-
Curso de Organismos Modelo en Biología Molecular Febrero 2025
El precio original era: $75.00.$57.00El precio actual es: $57.00. -
Masterclass: Dinámica y Composición de los Condensados Biomoleculares
El precio original era: $80.00.$60.00El precio actual es: $60.00.
Buscar
Últimos Posts
Últimos Comentarios
Categorías
Archivos
- marzo 2026 (5)
- febrero 2026 (15)
- enero 2026 (21)
- diciembre 2025 (20)
- noviembre 2025 (16)
- octubre 2025 (21)
- septiembre 2025 (17)
- agosto 2025 (17)
- julio 2025 (19)
- junio 2025 (24)
- mayo 2025 (26)
- abril 2025 (49)
- marzo 2025 (20)
- febrero 2025 (10)
- enero 2025 (7)
- diciembre 2024 (8)
- noviembre 2024 (23)
- octubre 2024 (7)
Palabras clave
Sígue las noticias
Te invitamos a registrar tus datos como tu correo electrónico para que puedas recibir las últimas noticias y anuncios de Biología Molecular México

By signing up, you agree to the our terms and our Privacy Policy agreement.