¡Tu carrito está actualmente vacío!
La Conexión Intestino-Tumor: Descubren Cómo una Bacteria Intestinal Dirige a las Células Inmunitarias para Potenciar la Inmunoterapia Contra el Cáncer
En Pocas Palabras:
La inmunoterapia con inhibidores de punto de control (ICB), como los que bloquean PD-1, ha revolucionado el tratamiento del cáncer, pero solo funciona en una minoría de pacientes. Se sabe que la microbiota intestinal influye en la respuesta, pero no se conocían los mecanismos exactos. Un nuevo estudio ha identificado una nueva cepa bacteriana, Hominenteromicrobium YB328, aislada de pacientes que respondieron bien a la terapia. Esta bacteria, al ser administrada a ratones, potencia drásticamente la eficacia de la inmunoterapia anti-PD-1. Lo hace activando en el intestino un tipo específico de células dendríticas (cDCs CD103+CD11b+), que actúan como “entrenadoras” del sistema inmune. Estas cDCs activadas migran desde el intestino hasta el tumor, donde “enseñan” a los linfocitos T CD8+ a reconocer y atacar eficazmente las células cancerosas. Este descubrimiento no solo identifica una bacteria beneficiosa clave, sino que desvela un mecanismo fundamental de cómo el intestino puede dirigir la respuesta inmune en tumores distantes.
El Enigma de la Inmunoterapia y el Papel del Microbioma
La inmunoterapia, y en particular los inhibidores de punto de control inmunitario (ICB) que bloquean la vía PD-1/PD-L1, ha transformado el panorama del tratamiento del cáncer, ofreciendo esperanzas a pacientes con tumores avanzados. Estos fármacos funcionan “quitando los frenos” al sistema inmunitario, permitiendo que los linfocitos T CD8+ reconozcan y destruyan las células cancerosas. Sin embargo, un gran enigma persiste: ¿por qué solo una fracción de los pacientes responde a estas terapias? En los últimos años, la comunidad científica ha descubierto una conexión sorprendente: la composición de la microbiota intestinal (la comunidad de billones de bacterias que viven en nuestro intestino) es un factor clave que predice la eficacia de la inmunoterapia. Pero, ¿cómo exactamente estas bacterias intestinales influyen en una batalla inmunitaria que se libra en un tumor lejano? Un estudio innovador publicado en la prestigiosa revista Nature por Nina Yi-Tzu Lin, Hiroyoshi Nishikawa y un equipo de investigadores de Japón, ha identificado una nueva cepa bacteriana y ha desvelado un elegante mecanismo de “comunicación a larga distancia” que explica esta crucial conexión intestino-tumor.

Identificando a los “Aliados” Microbianos: La Bacteria YB328
Los investigadores comenzaron analizando las heces de pacientes con cáncer que recibían terapia de bloqueo de PD-1. Descubrieron que los pacientes que respondían bien al tratamiento (respondedores) tenían una microbiota intestinal significativamente más diversa y estaban enriquecidos en ciertas familias de bacterias, como Ruminococcaceae. A partir de las muestras de estos pacientes, lograron aislar una nueva cepa bacteriana hasta ahora no descrita, que designaron como YB328, perteneciente al género Hominenteromicrobium.


Para probar su función, realizaron experimentos en ratones con tumores. Lo que encontraron fue extraordinario:
- Ratones que recibieron trasplantes fecales de pacientes respondedores mostraron una respuesta antitumoral mucho más fuerte a la terapia anti-PD-1 que aquellos que recibieron trasplantes de no respondedores.
- De manera crucial, la administración oral de la bacteria YB328 por sí sola en ratones fue suficiente para aumentar drásticamente la eficacia de la inmunoterapia anti-PD-1, inhibiendo el crecimiento tumoral.
- Incluso en ratones que habían recibido trasplantes fecales de pacientes no respondedores, la suplementación con YB328 fue capaz de “rescatar” la respuesta al tratamiento, demostrando que esta bacteria puede actuar de manera dominante para promover la inmunidad antitumoral.


El Mecanismo: Células Dendríticas como Mensajeras Migratorias
La gran pregunta era: ¿cómo lo hace YB328? El estudio desveló un mecanismo de acción paso a paso:
- Activación en el intestino: La bacteria YB328 interactúa con las células inmunes en el tejido linfoide asociado al intestino. Específicamente, estimula y promueve la maduración de un subtipo clave de células dendríticas convencionales (cDCs), las CD103+CD11b+.
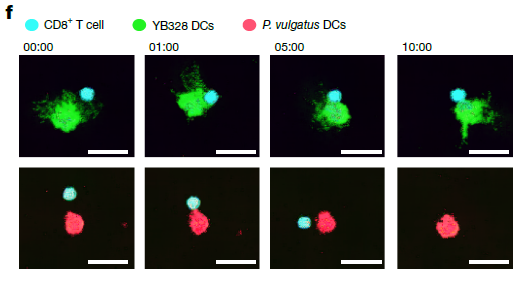
- Migración al Tumor: Estas cDCs, una vez “entrenadas” por YB328 en el intestino, no se quedan allí. Migran desde el intestino hasta los ganglios linfáticos que drenan el tumor y, finalmente, hasta el propio microambiente tumoral (TME).
- Entrenamiento de los linfocitos T: Una vez en el tumor, estas cDCs migratorias se convierten en las “instructoras” de élite de los linfocitos T CD8+. Presentan los antígenos tumorales a los linfocitos T de una manera mucho más eficaz, promoviendo su activación y su capacidad para reconocer y matar a las células cancerosas.
- Prolongación de la Interacción: Observaron que las cDCs activadas por YB328 se involucraban en interacciones más prolongadas y estables con los linfocitos T CD8+ específicos del tumor, asegurando una activación más robusta.
Esencialmente, YB328 actúa como el “sargento instructor” en el intestino, entrenando a un escuadrón de élite de células dendríticas que luego viajan al campo de batalla (el tumor) para dirigir a las “tropas” (los linfocitos T) de manera mucho más efectiva.

Confirmación en Pacientes Humanos
Para cerrar el círculo, los investigadores volvieron a los datos de pacientes. Encontraron una correlación directa y significativa: aquellos pacientes con una mayor abundancia de YB328 en su intestino tenían una mayor infiltración de estas cDCs CD103+CD11b+ en sus tumores y, a su vez, una respuesta clínica favorable a la terapia anti-PD-1 en diversos tipos de cáncer.
Implicaciones y Futuro: Hacia la “Bacterioterapia” de Precisión
Este estudio tiene implicaciones transformadoras para el futuro de la inmunoterapia contra el cáncer:
- Mecanismo Aclarado: Proporciona uno de los mecanismos más detallados hasta la fecha que explica cómo una bacteria comensal específica puede potenciar la inmunidad antitumoral sistémica.
- Nueva Generación de Probióticos: La bacteria YB328 se posiciona como un candidato principal para ser desarrollada como un “probiótico oncológico” o un producto bioterapéutico vivo. Podría administrarse a pacientes para mejorar su respuesta a la inmunoterapia.
- Estrategias para Superar la Resistencia: Podría ser una estrategia para convertir a los “no respondedores” a la inmunoterapia en “respondedores”, como se demostró en los experimentos de rescate en ratones.
- Biomarcadores Predictivos: La medición de la abundancia de YB328 en las heces podría servir como un biomarcador no invasivo para predecir qué pacientes tienen más probabilidades de beneficiarse del tratamiento con ICB.
Conclusión: Una Alianza Estratégica entre Microbios y Medicina
El trabajo de Lin, Nishikawa y su equipo es un hito en la comprensión de la intrincada conexión entre nuestra microbiota intestinal y la respuesta al cáncer. Al identificar a Hominenteromicrobium YB328 y desvelar su elegante mecanismo de acción a través de la activación y migración de células dendríticas, este estudio no solo resuelve una pieza clave del rompecabezas de la inmunoterapia, sino que también pavimenta el camino hacia una nueva era de la “bacterioterapia” de precisión. Nos acerca un paso más a un futuro en el que podamos modular de forma racional nuestra microbiota para mejorar drásticamente la eficacia de los tratamientos contra el cáncer.
Referencia del Artículo:
Lin, N. Y.-T., Fukuoka, S., Koyama, S., Motooka, D., Tourlousse, D. M., Shigeno, Y., … & Nishikawa, H. (2025). Microbiota-driven antitumour immunity mediated by dendritic cell migration. Nature. https://doi.org/10.1038/s41586-025-09249-8
AI bacterias Biología Sintética CRISPR cáncer envejecimiento Escherichia coli evolución Microbioma microbiota regulación resistencia salud VIH virus
Ultimos Productos
-
Curso de Organismos Modelo en Biología Molecular Febrero 2025
El precio original era: $75.00.$57.00El precio actual es: $57.00. -
Masterclass: Dinámica y Composición de los Condensados Biomoleculares
El precio original era: $80.00.$60.00El precio actual es: $60.00.
Buscar
Últimos Posts
Últimos Comentarios
Categorías
Archivos
- marzo 2026 (5)
- febrero 2026 (15)
- enero 2026 (21)
- diciembre 2025 (20)
- noviembre 2025 (16)
- octubre 2025 (21)
- septiembre 2025 (17)
- agosto 2025 (17)
- julio 2025 (19)
- junio 2025 (24)
- mayo 2025 (26)
- abril 2025 (49)
- marzo 2025 (20)
- febrero 2025 (10)
- enero 2025 (7)
- diciembre 2024 (8)
- noviembre 2024 (23)
- octubre 2024 (7)
Palabras clave
Sígue las noticias
Te invitamos a registrar tus datos como tu correo electrónico para que puedas recibir las últimas noticias y anuncios de Biología Molecular México

By signing up, you agree to the our terms and our Privacy Policy agreement.