En Pocas Palabras:
La bacteria Helicobacter pylori, famosa por causar úlceras gástricas, produce una proteína llamada CagA que inyecta en nuestras células para causar daño. Un nuevo estudio ha descubierto una función completamente inesperada y sorprendente para la CagA que no es inyectada: esta proteína es un potente inhibidor de la formación de amiloides. Los amiloides son agregados de proteínas anormales asociados a enfermedades neurodegenerativas como el Alzheimer (proteínas Aβ y tau) y el Parkinson (α-sinucleína), y también son cruciales para la formación de biopelículas bacterianas. Al bloquear la formación de estos agregados, la proteína CagA podría no solo interferir con otras bacterias competidoras, sino que también representa una molécula con un potencial terapéutico inesperado para tratar enfermedades de plegamiento de proteínas en humanos.

Un Villano Conocido con un Secreto Inesperado
La bacteria Helicobacter pylori es una de las “celebridades” del mundo microbiano, conocida por su notable capacidad de colonizar el hostil ambiente del estómago humano, afectando a cerca del 50% de la población mundial. Su presencia está asociada a una variedad de dolencias gastrointestinales, desde gastritis hasta úlceras pépticas y un mayor riesgo de cáncer gástrico. Una de sus principales armas es la proteína CagA (Cytotoxin-associated gene A), que la bacteria inyecta directamente en las células epiteliales del estómago para manipularlas y causar inflamación. Sin embargo, un nuevo y revolucionario estudio publicado en Science Advances por Zhen Jin, Gefei Chen y un equipo internacional de investigadores, ha revelado una faceta completamente inesperada y potencialmente beneficiosa de esta proteína: CagA es un inhibidor de amplio espectro y extraordinariamente potente de la formación de fibrillas amiloides.
El Doble Filo de los Amiloides: Funcionales y Patogénicos
Las fibrillas amiloides son estructuras altamente ordenadas formadas por la agregación de proteínas. Pueden ser:
- Funcionales: Muchas bacterias, como E. coli y Pseudomonas, utilizan amiloides (como las proteínas Curli y FapC, respectivamente) como un andamio estructural para construir biopelículas. Estas comunidades bacterianas son como “ciudades” blindadas que protegen a las bacterias de los antibióticos y del sistema inmune, siendo una causa principal de infecciones crónicas.
- Patogénicos: En humanos, la agregación anormal de ciertas proteínas en forma de amiloides es el sello distintivo de devastadoras enfermedades neurodegenerativas, como el Alzheimer (agregados de la proteína tau y el péptido Aβ), el Parkinson (agregados de α-sinucleína) y la diabetes tipo 2 (agregados de la hormona IAPP).
El Descubrimiento: CagA, el “Guardaespaldas” Anti-Amiloide
Los investigadores descubrieron que la porción N-terminal de la proteína CagA (CagA^N), que H. pylori también libera al exterior, tiene una asombrosa capacidad para detener la formación de amiloides:
- Inhibe Biopelículas Bacterianas: CagA^N fue capaz de inhibir eficazmente la formación de biopelículas de la bacteria Pseudomonas. Lo hizo bloqueando la formación de las fibrillas amiloides funcionales (FapC) que la bacteria necesita para construir su estructura protectora. Esto sugiere que H. pylori podría usar CagA como un arma para competir con otras bacterias en el microbioma, “desmantelando” sus defensas.

- Bloquea la Agregación Patogénica Humana: De manera aún más sorprendente, CagA^N demostró una potencia excepcional para inhibir la formación de los amiloides patogénicos humanos:
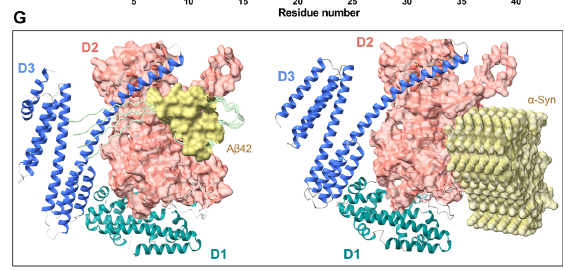
- Alzheimer: Inhibió la agregación tanto del péptido Aβ como de la proteína tau a concentraciones nanomolares, un nivel de eficacia mucho mayor que el de otras moléculas grandes. El análisis cinético reveló que CagA^N actúa en las primeras etapas de la nucleación de Aβ (evitando que los primeros agregados se formen) y sobre los procesos de nucleación secundaria y elongación de tau.
- Parkinson: También detuvo eficazmente la agregación de la α-sinucleína, principalmente al bloquear la elongación de las fibrillas. Las imágenes de microscopía mostraron que CagA^N se une a los extremos de las fibrillas de α-sinucleína, impidiendo que crezcan más.
- Diabetes Tipo 2: De igual forma, fue eficaz inhibiendo la formación de fibrillas de IAPP.

Mecanismo Específico y Selectivo
Es crucial destacar que CagA^N no actúa como una “chaperona” molecular general (proteínas que ayudan a otras a plegarse correctamente y evitan la agregación inespecífica). Su actividad es altamente específica contra la formación de amiloides. El estudio, utilizando predicciones estructurales de vanguardia con AlphaFold 3, sugiere que el dominio II de CagA^N es la región clave responsable de esta actividad anti-amiloide, interactuando directamente con las estructuras en formación.

Implicaciones y Futuro: Reevaluando a H. pylori
Este descubrimiento tiene implicaciones profundas y abre nuevas y emocionantes vías de investigación:
- Una Nueva Dimensión en las Interacciones Microbianas: Revela un mecanismo sofisticado por el cual H. pylori podría modular su microambiente, compitiendo con otras bacterias al desestabilizar sus biopelículas.
- Una Relación Compleja con las Enfermedades Neurodegenerativas: La asociación entre la infección por H. pylori y enfermedades como el Alzheimer ha sido objeto de debate, con resultados contradictorios. Este estudio plantea una posibilidad intrigante: si bien la infección puede promover la neuroinflamación, la proteína CagA liberada podría, paradójicamente, tener un efecto protector local al inhibir la agregación amiloide. Esto podría explicar algunas de las discrepancias y sugiere que la presencia de cepas CagA-positivas (más comunes en Asia Oriental que en Occidente) podría ser un factor a considerar.
- Potencial Terapéutico Inesperado: La proteína CagA, o específicamente su dominio II, emerge como un candidato a agente terapéutico de origen natural para una amplia gama de enfermedades de plegamiento de proteínas. Su alta potencia y su mecanismo de acción específico lo convierten en un modelo fascinante para el desarrollo de nuevos fármacos anti-amiloides.
Conclusión: De Villano a Potencial Héroe Inesperado
El estudio de Jin, Chen y su equipo transforma nuestra visión de la proteína CagA de H. pylori. Más allá de ser una toxina que causa daño gástrico, CagA es un potente y versátil inhibidor de amiloides, capaz de interferir tanto con las biopelículas bacterianas como con los agregados patogénicos que definen algunas de las enfermedades más devastadoras de nuestro tiempo. Este hallazgo no solo desvela una nueva capa de complejidad en la biología de H. pylori y su interacción con su entorno, sino que también nos proporciona una molécula natural con un potencial terapéutico asombroso, demostrando una vez más que el mundo microbiano es una fuente inagotable de soluciones ingeniosas a problemas biológicos complejos.
Referencia del Artículo:
Jin, Z., Olsen, W. P., Mörman, C., Leppert, A., Kumar, R., Møllebjerg, A., … & Chen, G. (2025). Helicobacter pylori CagA protein is a potent and broad-spectrum amyloid inhibitor. Science Advances, 11, eads7525. https://www.science.org/doi/10.1126/sciadv.ads7525