Dentro del núcleo de cada una de nuestras células, dos metros de ADN están empaquetados en un espacio mil veces más pequeño que la cabeza de un alfiler. Este increíble acto de contorsionismo no es aleatorio; es una coreografía precisa y dinámica que determina qué genes se encienden o se apagan, definiendo si una célula se convertirá en una neurona, una célula de la piel o un glóbulo rojo. Durante décadas, los científicos han sabido que los “interruptores” genéticos (llamados enhancers) deben tocar físicamente los genes que controlan (los promotores), a menudo a lo largo de vastas distancias del genoma. Pero ¿cómo se produce exactamente este contacto? Un estudio revolucionario, publicado en la prestigiosa revista Cell, ha logrado visualizar esta interacción con una resolución sin precedentes, a nivel de un solo par de bases de ADN, revelando un modelo unificado que explica cómo las leyes de la física y la bioquímica orquestan la estructura del genoma y la regulación génica.

1. El Desafío: Ver el ADN a la Máxima Resolución
Imagina intentar entender cómo funciona un motor de coche mirando una foto borrosa desde lejos. Eso es, en esencia, lo que los científicos podían hacer hasta ahora. Las técnicas existentes para mapear la estructura 3D del genoma, como el Hi-C, ofrecían una visión a escala de “barrios” o “ciudades” del genoma, pero no podían resolver los detalles a nivel de “casas” individuales, es decir, de los pequeños elementos reguladores donde se unen las proteínas. Era imposible ver cómo interactuaban las piezas más pequeñas.
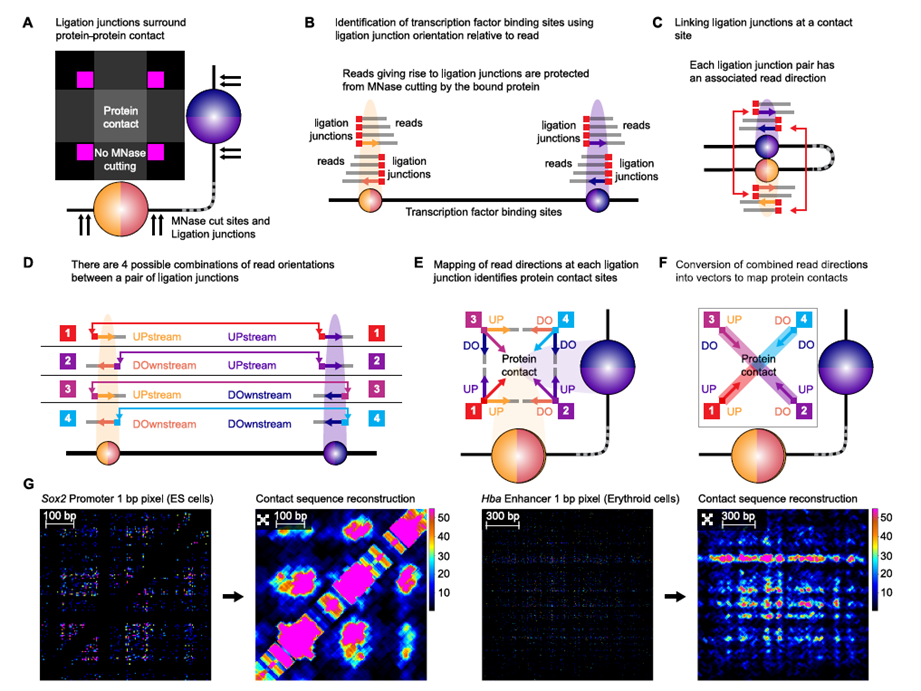
Para superar esta barrera, un equipo de la Universidad de Oxford desarrolló una técnica ultrapotente llamada Micro Capture-C ultra (MCCu). Esta tecnología permite generar mapas de contacto del genoma con una resolución de un solo par de bases, lo que representa un aumento de mil veces en la precisión respecto a los métodos anteriores. Es como pasar de un mapa de carreteras a una imagen satelital de ultraalta definición donde se puede ver cada coche en la calle.

Lo más importante: La nueva técnica MCCu ha permitido, por primera vez, visualizar la estructura 3D de la cromatina a la escala de los propios factores de transcripción y nucleosomas, revelando la arquitectura íntima de los elementos que controlan los genes.
2. La Arquitectura a Nanoescala: Dominios, Bucles y Contactos Específicos
Con esta nueva visión, los investigadores descubrieron una organización mucho más compleja de lo que se imaginaba. Observaron que la cromatina no es una masa uniforme, sino que está particionada en “dominios a nanoescala”: pequeños glóbulos de cromatina compacta, separados entre sí por regiones abiertas y accesibles llamadas “regiones desprovistas de nucleosomas” (NDRs).
Es en estas regiones abiertas (las NDRs) donde se sientan los interruptores genéticos (enhancers y promotores) y las proteínas que los regulan (factores de transcripción). El hallazgo clave fue que estas NDRs no interactúan al azar. En lugar de formar un “gran tazón de espaguetis”, se observó que las NDRs de los enhancers y los promotores establecen contactos físicos muy precisos y localizados entre sí, como si se buscaran específicamente en el espacio nuclear abarrotado.

Lo más importante: La cromatina está organizada en pequeños dominios compactos, y los elementos reguladores (enhancers y promotores) se encuentran en regiones abiertas que se buscan y contactan entre sí con una precisión asombrosa, formando el circuito de la regulación génica.
3. La Física detrás de la Biología: Un Modelo Unificado Impulsado por la Biofísica
¿Qué fuerza impulsa esta organización? Para responder a esto, el equipo combinó sus datos experimentales con simulaciones de dinámica molecular. Crearon un modelo computacional que simulaba el comportamiento de la cromatina basándose únicamente en sus propiedades fisicoquímicas: la rigidez del ADN, las cargas eléctricas de las proteínas (histonas) y las modificaciones químicas como la acetilación.

Sorprendentemente, la simulación reprodujo casi a la perfección los mapas de contacto observados en las células vivas. Esto los llevó a proponer un modelo unificado donde la biofísica es la principal fuerza orquestadora:
- Condensación por Defecto: Los nucleosomas (las “perlas” de proteína alrededor de las cuales se enrolla el ADN) tienden a agruparse entre sí, formando los dominios a nanoescala compactos.
- Repulsión y Separación: Las regiones abiertas (NDRs), al carecer de nucleosomas, son más flexibles y cargadas negativamente, lo que hace que sean “expulsadas” de estos cúmulos compactos.
- Coalescencia en la Superficie: Estas NDRs expulsadas tienden a encontrarse y coalescer en la “superficie” de los dominios de cromatina, facilitando el contacto entre enhancers y promotores.
- El Papel de la Acetilación: Las modificaciones químicas como la acetilación de histonas neutralizan las cargas positivas, haciendo que la cromatina se “hinche” y se vuelva menos compacta, ayudando a estabilizar estas regiones activas en la interfaz.
Lo más importante: La estructura del genoma no está dictada por un complejo código de reconocimiento, sino por principios biofísicos simples. Las regiones de ADN sin nucleosomas son “expulsadas” de la cromatina compacta y se encuentran en un espacio común, lo que facilita la comunicación entre enhancers y promotores.
4. Confirmando el Modelo: Eliminando las Piezas Clave
Para probar su modelo, los científicos utilizaron la ingeniería genética para eliminar proteínas clave de la célula. Al eliminar factores de transcripción como SOX2, observaron que las regiones abiertas (NDRs) donde este se unía “colapsaban”, los nucleosomas volvían a ocupar ese espacio y los contactos a larga distancia con los promotores desaparecían. Esto confirmó que la presencia de factores de transcripción es crucial para mantener estas regiones abiertas y funcionales.
De manera similar, al eliminar componentes del complejo Mediador (una maquinaria molecular que actúa como puente entre enhancers y promotores), vieron que los contactos a gran escala se mantenían, pero la arquitectura fina dentro del promotor se desorganizaba, impidiendo la activación del gen.

Lo más importante: Los experimentos de “eliminación” de proteínas clave validaron el modelo: los factores de transcripción son esenciales para crear y mantener las regiones abiertas, y el complejo Mediador actúa para estabilizar las interacciones precisas en el promotor, no como un ancla estructural a gran escala.
5. Una Nueva Visión de la Regulación Génica
Este trabajo transforma nuestra comprensión de cómo se organiza y funciona el genoma. Nos aleja de la idea de un sistema rígido de “cerraduras y llaves” y nos acerca a un modelo mucho más dinámico y fluido, gobernado por las propiedades biofísicas de sus componentes. Es un elegante recordatorio de que las complejas funciones de la vida a menudo emergen de reglas físicas sorprendentemente simples. Esta nueva visión a escala de pares de bases no solo resuelve un enigma fundamental de la biología, sino que también proporciona un marco para entender cómo las mutaciones en regiones no codificantes pueden alterar esta delicada coreografía y causar enfermedades.
Referencia:
Li, H., Dalgleish, J. L. T., Lister, G., Collepardo-Guevara, R., Milne, T. A., & Davies, J. O. J. (2025). Mapping chromatin structure at base-pair resolution unveils a unified model of cis-regulatory element interactions. Cell, 188, 1-19. https://doi.org/10.1016/j.cell.2025.10.013