¡Tu carrito está actualmente vacío!
Crean el Primer Atlas 3D del “Segundo Cerebro” en el Intestino
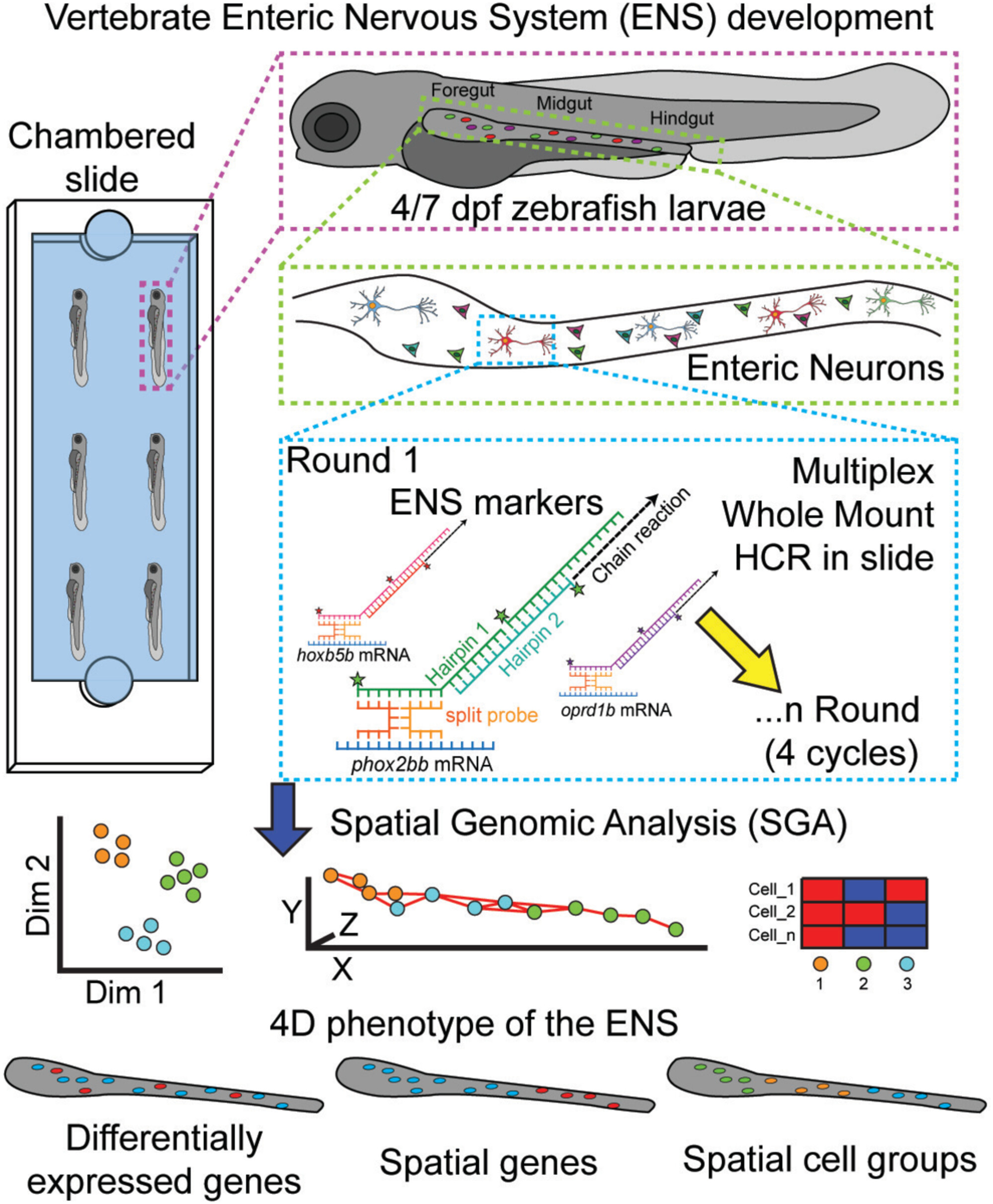
Imaginen por un momento un cerebro. No el que reside en nuestro cráneo, sino uno distribuido, una red increíblemente compleja de millones de neuronas que tapiza las paredes de nuestro sistema digestivo. Este no es un cerebro cualquiera; es el Sistema Entérico Nervioso (SEN), a menudo apodado nuestro “segundo cerebro”. Funciona con una autonomía asombrosa, orquestando funciones vitales como la digestión, la absorción de nutrientes y la motilidad intestinal, sin necesidad de recibir órdenes directas del cerebro principal. Pero, ¿cómo se construye esta maravilla biológica? ¿Cómo saben millones de células dónde ir, en qué tipo de neurona convertirse y cómo conectarse para formar una red funcional a lo largo de metros de intestino? Este ha sido uno de los grandes misterios de la biología del desarrollo. Hoy, gracias a un innovador estudio publicado en The FASEB Journal por el equipo de Rodrigo Moreno-Campos y Rosa A. Uribe de la Universidad de Rice, estamos más cerca que nunca de tener la respuesta. Utilizando una tecnología de vanguardia llamada Análisis Genómico Espacial (SGA), han logrado lo que parecía ciencia ficción: crear el primer atlas genómico en tres dimensiones que muestra, célula por célula, cómo el SEN se organiza y especializa durante su desarrollo.
El SEN no es solo un simple controlador de la digestión; es un centro de comando sofisticado. Su complejidad es tal que fallos en su desarrollo pueden tener consecuencias devastadoras, dando lugar a trastornos gastrointestinales graves. La más conocida de estas afecciones es la enfermedad de Hirschsprung, un trastorno congénito en el que partes del intestino carecen de neuronas, lo que impide el movimiento peristáltico y provoca obstrucciones severas. Entender cómo se forma el SEN no es, por tanto, una mera curiosidad académica, sino una necesidad imperiosa para desarrollar futuras terapias. El problema fundamental ha sido la dificultad de observar este proceso en su totalidad. El desarrollo es un ballet cuatridimensional: ocurre en un espacio tridimensional (largo, ancho y profundidad del intestino) y a lo largo del tiempo. Las técnicas tradicionales a menudo nos obligaban a elegir: podíamos analizar la expresión génica de miles de células individuales, pero perdiendo su ubicación original (como analizar los ingredientes de un batido sin saber de qué fruta provenían), o podíamos ver la estructura del tejido, pero con información molecular muy limitada. El estudio de Moreno-Campos y su equipo rompe estas barreras, ofreciendo una visión integral que combina la identidad molecular de cada célula con su ubicación precisa en el espacio, creando un mapa vivo y detallado del desarrollo.
Para lograr esta hazaña, los investigadores recurrieron a un modelo animal excepcional: el pez cebra. Este pequeño pez tropical es una superestrella en los laboratorios de biología del desarrollo por varias razones. Sus larvas son transparentes, lo que permite a los científicos observar directamente el desarrollo de sus órganos internos en un animal vivo. Su desarrollo es increíblemente rápido; procesos que en mamíferos tardan semanas, en el pez cebra ocurren en cuestión de días. Además, compartimos una sorprendente cantidad de genes y vías moleculares con ellos, lo que significa que los descubrimientos hechos en el pez cebra a menudo son directamente relevantes para la salud humana. El SEN del pez cebra, aunque más simple que el nuestro (carece de uno de los dos plexos neuronales que tenemos los mamíferos), sigue los mismos principios fundamentales de desarrollo, convirtiéndolo en un sistema ideal para descifrar los mecanismos centrales de su formación. El equipo se centró en dos momentos clave: los 4 y los 7 días después de la fertilización (dpf), etapas que representan una fase temprana y una más tardía de la diferenciación neuronal en el intestino del pez.
La tecnología que está en el corazón de este estudio es una sinfonía de técnicas avanzadas. El primer movimiento fue visualizar los genes en acción dentro del intestino intacto de las larvas de pez cebra. Para ello, utilizaron una técnica llamada Reacción en Cadena por Hibridación (HCR) de montaje completo y multiplexada. En lugar de mirar un solo gen a la vez, la HCR les permitió “pintar” simultáneamente tres ARNm (moléculas que indican que un gen está activo) con diferentes colores fluorescentes. Lo verdaderamente ingenioso fue el enfoque secuencial: después de capturar imágenes en 3D de alta resolución con un microscopio confocal, aplicaban un tratamiento que borraba las señales fluorescentes sin dañar el tejido, dejando el escenario listo para una nueva ronda de “pintura” con otros tres genes. Repitieron este ciclo cuatro veces, permitiéndoles mapear la expresión de 12 genes clave del SEN en las mismas células exactas. Estos 12 genes no fueron elegidos al azar; representan un espectro de funciones, desde marcadores de células progenitoras neurales (las “células madre” del SEN) hasta marcadores de neuronas ya diferenciadas y funcionales.
Con estas pilas de imágenes tridimensionales multicolores, llegó el segundo movimiento: la interpretación de los datos. Aquí es donde la inteligencia artificial y la bioinformática tomaron el protagonismo. Utilizando un software avanzado llamado IMARIS, los investigadores segmentaron las imágenes para identificar cada una de las células del SEN de forma individual. A cada célula se le asignó una identidad única, con sus coordenadas exactas (X, Y, Z) en el intestino y un perfil de expresión génica basado en la intensidad de las señales fluorescentes de los 12 genes analizados. Este proceso, realizado para múltiples larvas en ambas etapas de desarrollo (4 y 7 días), generó una cantidad masiva de datos. El verdadero Análisis Genómico Espacial (SGA) comenzó al integrar toda esta información utilizando una plataforma computacional llamada Giotto. Este software fue capaz de analizar simultáneamente los perfiles genéticos y las posiciones espaciales de miles de células de diferentes individuos y etapas, corrigiendo las variaciones entre muestras y revelando los patrones ocultos en la complejidad de los datos. El resultado final fue un mapa dinámico y multidimensional: un atlas que no solo muestra dónde están las células, sino también quiénes son a nivel molecular y cómo cambian con el tiempo.
Los descubrimientos que emergieron de este atlas digital son profundos y revelan una regionalización molecular exquisita. Al agrupar las células basándose en la similitud de su expresión génica y su ubicación, el algoritmo de agrupamiento Leiden identificó 12 comunidades celulares distintas. Estas comunidades no estaban distribuidas al azar. Las células de las larvas de 4 días (la etapa temprana) formaban predominantemente los grupos del 1 al 4, mientras que las de 7 días (la etapa tardía) constituían principalmente los grupos del 5 al 12. Esto demostró una clara progresión en el desarrollo, donde la identidad molecular de las células del SEN evoluciona significativamente en tan solo tres días. Al analizar qué genes definían cada grupo (los llamados genes diferencialmente expresados o DEGs), encontraron firmas moleculares claras. Por ejemplo, los genes hoxb5b y hoxa4a, conocidos por ser “genes arquitectos” que definen la identidad posicional en el embrión, estaban muy activos en los grupos tempranos (1-4). En contraste, genes como etv1, asociado con la maduración neuronal, eran característicos de los grupos más tardíos (5-12). Esto sugiere que el programa genético del SEN pasa de una fase de “establecimiento del plan corporal” a una de “especialización y funcionalidad”.
Más allá de clasificar las células, el análisis espacial permitió a los investigadores construir la red de interacciones celulares, el “tejido social” del SEN. Al analizar la proximidad física entre las diferentes comunidades celulares, pudieron modelar cómo interactúan. Los resultados mostraron que a los 4 días, la red era más simple, con algunas interacciones fuertes entre grupos específicos, como el 2 y el 3. Sin embargo, a los 7 días, el panorama cambiaba drásticamente. Aunque la fuerza de las interacciones individuales entre algunos grupos podía ser menor, el número total de conexiones se disparaba, creando una red mucho más densa e interconectada. Esto es un reflejo visual y cuantitativo de la maduración del SEN: lo que comienza como una cadena de células más dispersa se convierte en una red neuronal integrada y compleja, capaz de coordinar las sofisticadas funciones del intestino maduro. La estructura de la red también reveló que algunos grupos celulares prefieren interactuar con células de su mismo tipo (interacciones homotípicas), mientras que otros se especializan en conectar diferentes tipos de células (interacciones heterotípicas), un hallazgo crucial para entender cómo se establece la circuitería neuronal.
Quizás el hallazgo más fascinante fue la identificación de “genes espacialmente variables” (SVGs), genes cuya expresión no es uniforme, sino que forma patrones geográficos definidos a lo largo del eje del intestino. El análisis reveló patrones sorprendentes que sugieren una división del trabajo molecular. Uno de los ejemplos más claros fue el contraste entre los genes ret y etv1 en la etapa de 7 días. El gen ret es un receptor crucial para la migración y supervivencia de las células progenitoras del SEN. El estudio mostró que su expresión estaba fuertemente enriquecida en la parte más posterior del intestino, el llamado “frente de onda” donde las células aún están colonizando el territorio. Esto tiene un perfecto sentido biológico: ret está guiando la expansión del SEN. En un contraste casi perfecto, el gen etv1, implicado en la diferenciación de tipos neuronales específicos, se encontraba predominantemente en las regiones anteriores y medias del intestino (el prointestino y el intestino medio), zonas que ya han sido colonizadas y donde las neuronas están madurando. Esta binarización espacial sugiere que existen diferentes programas de desarrollo ocurriendo simultáneamente en distintas regiones del intestino: mientras la parte trasera se enfoca en la expansión, la delantera se enfoca en la especialización. Esta es la regionalización molecular en su máxima expresión, un principio organizativo fundamental que ahora puede ser estudiado con un detalle sin precedentes.
Las implicaciones de este trabajo son inmensas y trascienden la biología del pez cebra. Este atlas 3D del desarrollo del SEN proporciona un mapa de referencia, una “plantilla de la normalidad”. Ahora, los científicos pueden empezar a investigar qué sale mal en modelos de enfermedades como la de Hirschsprung. ¿Es un fallo en la migración de las células que expresan ret? ¿Se detiene prematuramente la expresión de los genes Hox? ¿No se activan los genes de diferenciación como etv1 en el lugar correcto? Con esta nueva herramienta, se pueden abordar estas preguntas a nivel de una sola célula y en su contexto tridimensional. Este conocimiento es el primer paso para diseñar intervenciones más inteligentes. Si entendemos las vías moleculares exactas que fallan, podríamos, en un futuro, pensar en terapias que reactiven genes específicos o proporcionen las señales moleculares que faltan para restaurar el desarrollo normal del SEN. Además, este estudio establece un nuevo estándar técnico y conceptual. El marco de Análisis Genómico Espacial desarrollado aquí puede aplicarse para estudiar el desarrollo de cualquier otro órgano, desde el corazón hasta el cerebro, desvelando los principios universales de cómo se construye la vida, una célula a la vez. En resumen, el trabajo de Moreno-Campos y Uribe no solo nos ha dado una imagen espectacularmente bella del “segundo cerebro” en formación, sino que nos ha proporcionado una nueva forma de mirar, y de entender, la compleja coreografía de la vida misma.
A continuación les dejamos el enlace de está noticia en donde el miembro de nuestro equipo Rodrigo Moreno Campos fue parte de esta investigación. CLIC AQUI
AI bacterias Biología Sintética CRISPR cáncer envejecimiento Escherichia coli evolución Microbioma microbiota regulación resistencia salud VIH virus
Ultimos Productos
-
Curso de Organismos Modelo en Biología Molecular Febrero 2025
El precio original era: $75.00.$57.00El precio actual es: $57.00. -
Masterclass: Dinámica y Composición de los Condensados Biomoleculares
El precio original era: $80.00.$60.00El precio actual es: $60.00.
Buscar
Últimos Posts
Últimos Comentarios
Categorías
Archivos
- marzo 2026 (5)
- febrero 2026 (15)
- enero 2026 (21)
- diciembre 2025 (20)
- noviembre 2025 (16)
- octubre 2025 (21)
- septiembre 2025 (17)
- agosto 2025 (17)
- julio 2025 (19)
- junio 2025 (24)
- mayo 2025 (26)
- abril 2025 (49)
- marzo 2025 (20)
- febrero 2025 (10)
- enero 2025 (7)
- diciembre 2024 (8)
- noviembre 2024 (23)
- octubre 2024 (7)
Palabras clave
Sígue las noticias
Te invitamos a registrar tus datos como tu correo electrónico para que puedas recibir las últimas noticias y anuncios de Biología Molecular México

By signing up, you agree to the our terms and our Privacy Policy agreement.